Сгорание - углеводород
Cтраница 1
Сгорание углеводородов является высо-коэкзотермичным процессом. Поэтому углеводороды главным образом сжигают с целью получения энергии. Ненасыщенные алифатические углеводороды-алкены ( оле-фины) и алкины ( ацетилены) - легко вступают в реакции присоединения по кратным углерод-углеродным связям. В отличие от них ароматические углеводороды с трудом вступают в реакции присоединения. Разновидностью присоединения является реакция полимеризации алкенов, которая позволяет получать множество ценных синтетических материалов. [1]
Сгорание углеводородов топлив протекает значительно сложнее, чем сгорание элементов, их составляющих. [2]
Теплота сгорания углеводорода зависит от содержания в молекуле водорода и от соотношения углерод: водород. [3]
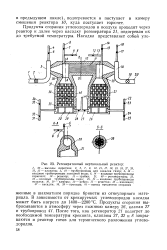 |
Регенеративный вертикальный реактор. [4] |
Продукты сгорания углеводородов в воздухе проходят через реактор и далее через насадку регенератора 21, подогревая их до требуемой температуры. [5]
Теплота сгорания углеводородов повышается по мере увеличения числа атомов углерода в молекуле. С увеличением числа атомов в молекуле предельных углеводородов возрастают также их плотность и температура кипения. [6]
Теплота сгорания углеводорода зависит от содержания в молекуле водорода и от соотношения углерод; водород. Чем больше в молекуле атомов водорода, тем выше теплота сгорания; наивысшей теплотой сгорания ( в расчете на единицу массы) обладают алканы, наименьшей - арены. [7]
Теплота сгорания углеводородов сильно зависит от молекулярного веса: чем тяжелее углеводород, тем больше его теплота сгорания. [8]
Теплота сгорания углеводорода зависит от содержания в молекуле водорода и от соотношения углерод: водород. Чем больше в молекуле атомов водорода, тем выше теплота сгорания; наивысшей теплотой сгорания ( в расчете на единицу массы) обладают алканы, наименьшей - арены. [9]
Скорость сгорания углеводородов, в зависимости от их строения и от принадлежности к тому или иному классу, различна. [10]
Скорость сгорания углеводородов в зависимости от их строения и от принадлежности к тому или иному классу, различна. [11]
При сгорании углеводорода происходит смещение электронов от атомов углерода и водорода к атомам кислорода, в результате чего атомы углерода и водорода становятся электроположительными и соединяются с электроотрицательными атомами кислорода. [12]
При сгорании углеводорода энергия уменьшается, ее избыток выделяется в виде тепла и света. А энтропия, мера неупорядоченности, действительно увеличивается, так как малые молекулы HjO и СО2 менее упорядочены в смысле расположения атомов, чем большая моло-кула углеводорода, скажем бутана. [13]
При сгорании углеводорода энергия уменьшается, ее избыток выделяется в виде тепла и света. А энтропия, мера неупорядоченности, действительно увеличивается, так как малые молекулы НУЭ и СО2 менее упорядочены в смысле расположения атомов, чем большая молекула углеводорода, скажем бутана. [14]
При сгорании углеводородов п основном образуются СОЕ, СО и НгО, тогда как при взрыве их - преимущественно атомы Ни радикалы ОМ. Лснксром по было обнаружено, что в процессе окисления углеводородов, например этилена, п качестве побочных продуктов получаются перекись водорода и диоксиметилперекись. Он полагал, что первично происходит присоединение кислорода к этилену, СгШ - J - О. Ii: О2; это вещество распадается затем либо на две молекулы формальдегида по уравнению Cali O. [15]
Страницы: 1 2 3 4