Более высокое значение - энергия - активация
Cтраница 3
Так, например, константы скорости щелочного гидролиза метоксиметилфторфосфоната и изопропоксиметилфторфосфо-ната равны 106 и 25 8 л / моль - сек соответственно. Сравнивая полученные данные, Ларссон предположил [113], что увеличение положительного индуктивного эффекта алкильной цепи алкокси-группы при переходе от метила к изопропилу приводит к увеличению электронной плотности у атома фосфора. Однако более высокое значение энергии активации щелочного гидролиза метоксиметилфторфосфоната ( 10 5 ккал / моль) по сравнению с изопропоксиметил-фторфосфонатом ( 9 1 ккал / моль) находится в противоречии с этим предположением. Из вышеизложенных представлений следует, что повышение энергии активации в реакциях нуклеофильного замещения у тетраэдрического атома фосфора, скорее всего, может быть объяснено возможностью рл - с - сопряжения алкоксигруппы с Sd-орбитами фосфора в переходном состоянии. Следовательно, можно предположить, что увеличение энергии активации в случае метилового аналога, по-видимому, связано с возможностью участия метильной группы в гиперконъюгации с реакционным центром в переходном состоянии. [31]
Исследование кинетики превращения С-центров в Л - центры под действием температуры показало, что она хорошо описывается феноменологическим уравнением Авраами, которое широко используется для описания процессов распада твердых пересыщенных растворов. Величина параметра процесса п свидетельствует о сферической форме Л - центров, или о прямоугольной и округлой формах пластин. Обращают на себя внимание более высокое значение энергии активации и низкая скорость процесса превращения С-центров в Л - центры. Причиной этого могут быть прежде всего структурные отличия исследованных алмазов. В частности, включения металла-растворителя в зависимости от их количества, размеров и распределения могут заметно видоизменять процессы диффузии примесных атомов, являясь эффективными стоками избыточных вакансий. Это влияние может усугубляться тем, что в ходе термической обработки, как показали визуальные наблюдения, идут процессы миграции и агрегации включений металла в кристалле. [33]
Величины энергии активации изменяются в различных опытах от 53 400 до 67 200 - кал и значения С от 29 до 33 в температурных пределах от 400 до 6009 С. Энергия активации уменьшается с повышением температурь кипения продукта. При одинаковом молекулярном весе ароматические продукты имеют более высокие значения энергии активации, чем парафинистые продукты. [34]
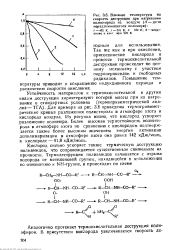 |
Влияние температуры на скорость деструкции при нагревании полистирола иа воздухе ( А - дотя неразложившегося полимера. 1 - 4ТО К. 2 - 520 К. 3 570 К. - иагре-еапне ь езот при 570 К. [35] |
Для примера на рис. 3.6 приведены термогравиметрические кривые разложения полистирола в атмосфере азота и кислорода воздуха. Из рисунка видно, что кислород ускоряет разложение полимера. Более высокая термостойкость полистирола в атмосфере азота по сравнению с кислородом подтверждается также более высоким значением энергии активации деполимеризации в атмосфере азота она равна 142 кДж / моль, в кислороде - 41 8 кДж / моль. [36]
Определенный выше характер функции распределения вполне согласуется с изменениями скорости реакции и энергии активации с заполнением. Действительно, в начале процесса происходит распад метанола, адсорбированного на наиболее активных участках. При этом, по мере течения реакции, контролирующая полоса быстро передвигается в сторону более высоких значений энергии активации, и происходит резкое снижение скорости. [37]
Из уравнения (186.1) видно, что между lni - ц и 1Т существует линейная зависимость и что по тангенсу угла наклона прямой можно рассчитать энергию активации. Если энергия активации практически не зависит от перенапряжения ( рис. 179, прямые а) и совпадает с величиной, специфической для процессов диффузии в водных растворах ( 10 - 12 кДж / моль), то электродная реакция сопровождается диффузионным перенапряжением. Более высокое значение энергии активации Е ( 40 - 80 кДж / моль), характерное для химических реакций в растворах, и зависимость Е от перенапряжения ( рис. 179, прямые б) свидетельствуют об активационной поляризации. [38]
Из уравнения (186.1) видно, что между 1ш т) и 1 / 7 существует линейная зависимость и что по тангенсу угла наклона прямой можно рассчитать энергию активации. Если энергия активации практически не зависит от перенапряжения ( рис. 179, прямые а) н совпадает с величиной, специфической для процессов диффузии в водных растворах ( 10 - 12 кДж / моль), то электродная реакция сопровождается диффузионным перенапряжением. Более высокое значение энергии активации Е ( 40 - 80 кДж / моль), характерное для химических реакций в растворах, и зависимость Е от перенапряжения ( рис. 179, прямые б) свидетельствуют об активационной поляризации. [39]
Из этого следует, что, как показано на рис. 4, доля прочно связанного водорода для рубина в гораздо меньшей степени зависит от температуры адсорбции, чем для сапфира. Это объясняет также, почему объем прочно связанного водорода одинаков для сапфира и рубина, если адсорбцию проводят при 250 С. В данном случае скорость процесса лимитируется стадией первичной адсорбции, для которой величина предэкспоненциального фактора чрезвычайно мала. Однако при адсорбции при 20 С более высокое значение энергии активации стадии миграции и связывания водорода на сапфире делают эту стадию лимитирующей, и объемы прочно связанного водорода на рубине и на сапфире делаются различными. В связи с этим необходимо допустить, что в действительности стадия миграции является быстрой, а различия между сапфиром и рубином связаны со стадией фиксации водорода, которая для рубина вызывает падение скорости пара-орто-превращения водорода по магнитному механизму. [40]
Дальнейшее декатионирование приводит к увеличению числа сильнокислых центров, однако общее число кислотных центров возможно падает. Если в реакции дегидратации изопропанола принимает участие широкий спектр кислотных центров, то при этом вполне возможно падение константы скорости. Проверка этого предположения может быть сделана при изучении кислотности цеолитов. Действительно, как было видно на рис. 4, энергетический спектр кислотных центров образца со степенью декатионирования 85 % начинается с более высоких значений энергий активации десорбции аммиака ( 32 ккал / моль), чем энергетический спектр образца со степенью декатионирования 30 %, однако в области покрытия поверхности аммиаком, большей 0 4 ммоль / г, уровни кривых меняются положениями. При переходе от 30 % - ного образца к образцу со степенью декатионирования, равной 85 %, наблюдается значительное увеличение количества сильных кислотных центров, способных необратимо хемосорбировать NH3 при высоких температурах ( см. рис. 5), но одновременно можно заметить и уменьшение количества более слабых центров, способных необратимо хемосорбировать NH3 при температурах - 180 - 190 С и ниже. [41]
До сих пор, чтобы как можно меньше усложнять картину, обсуждение ограничивалось процессами, в которых от восстановителя к окислителю переносился один электрон. Большинство рассматриваемых примеров затрагивало комплексы переходных металлов, устойчивые степени окисления которых отличаются на единицу. Поэтому закономерен вопрос: может ли за один акт окисления-восстановления переноситься больше одного электрона. Если реакция идет по внешнесферному механизму, ограничение Франка-Кондона ( соответствие энергий окислителя и восстановителя до переноса электронов) будет намного более серьезным, когда дело касается переноса двух электронов; и более высокие значения энергий активации и меньшая вероятность успешного окислительно-восстановительного столкновения приведут к тому, что процесс этот станет маловероятным. Если реакция идет в растворе, ограничения могут быть, по-видимому, смягчены по той причине, что реагенты могут находиться в тесном соприкосновении друг с другом ( в сольватационной ловушке) достаточно долго, для того чтобы участвовать в двух последовательных актах переноса электронов. Если реагирующие промежуточные соединения не живут столь долгое время, чтобы их можно было обнаружить, этот тип процесса, вероятно, нельзя будет по-настоящему отличить от синхронного переноса двух электронов. В реакции, протекающей по внутрисферному механизму, мостиковая связь может сохраняться достаточно долго, и поэтому возможен последовательный перенос более чем одного электрона. [42]
Как и для всех сшитых эластомеров при более высоких температурах ( выше 80 С) наблюдался шестой максимум, соответствующий 5-процессу химической релаксации. Значения энергии активации U и предэкспоненциального коэффициента В, определенные из данных рис. 8.6 для различных релаксационных процессов СК. С-ЗОА, приведены в табл. 3.1. Как следует из этих данных, для а - процесса коэффициент Б4 8 - 10 - 12, что совпадает со значением этого коэффициента в а-процессе ( гл. Из этого можно заключить, что кинетической единицей в а - процессе является сегмент. Тот факт, что а - процессу соответствуют более высокие значения главного времени релаксации по сравнению с - процессом, а значит при равенстве предэкспоненциального члена В - более высокое значение энергии активации, объясняют тем, что сегментальная подвижность в адсорбированном слое полимера затруднена. При понижении температуры [76] вначале теряется подвижность сегментов в связанном полимере ( твердой составляющей), что проявляется в виде максимума потерь, а затем в несвязанном полимере ( мягкой составляющей) - ос-максимум потерь. [43]
Страницы: 1 2 3
