Двухвалентная сера
Cтраница 1
Двухвалентная сера обычно окисляется, по крайней мере при комнатной температуре, лишь до сульфоокиси, но не до сульфона. На дифенилендисульфид и тетранитродифенил-дисульфид перекись водорода не действует. [1]
Двухвалентная сера, помимо проявления ослабленного индуктивного и 7Уг - эффектов, также способна в случае одинарной связи вызывать дело-кализацию электронов, направленную к атому серы, и это связано с наличием d - AO. Одним из условий, при которых может произойти делокализа-ция заряда, является наличие вакантной орбитали по соседству со свободной парой, подходящим образом ориентированной, или с я-электронами ( гл. Вполне достаточно, чтобы имелась орбиталь достаточно низкой энергии, такая, как вакантная АО главного квантового уровня, занимаемая самими валентными электронами, и 3d - AO атома серы удовлетворяют этому условию. В соответствии с этим имеются данные, основанные на различных фактах, подтверждающие представление о том, что 3d - АО ( или гибридизованные 3d - АО) атома серы способны стабилизовать, а следовательно, и облегчать образование как свободнорадикальных, так и карбанионных систем. Так, установлено, что в длинной цепи полисульфида внутренние связи S - S могут быть легче разорваны гемолитическим путем, чем связи S - SB более коротких полисульфидных цепях. Возможно, что в более длинных радикалах R - ( S) x - S интенсивность делокализации неспаренного электрона больше. Интересно отметить также, что довольно высокая энергия диссоциации [ в среднем - 60 ккал / моль ( 251 21 - 103 Дж / моль) ] для связи S - SB дисульфиде может быть отчасти связана с делокализацией свободной пары электронов серы между двумя атомами серы. [2]
Двухвалентная сера, помимо проявления ослабленного индуктивного и - f - Af-эффектов, также способна в случае одинарной связи вызывать дело-кализацию электронов, направленную к атому серы, и это связано с наличием d - AO. Одним из условий, при которых может произойти делокализа-ция заряда, является наличие вакантной орбитали по соседству со свободной парой, подходящим образом ориентированной, или с я-электронами ( гл. Вполне достаточно, чтобы имелась орбиталь достаточно низкой энергии, такая, как вакантная АО главного квантового уровня, занимаемая самими валентными электронами, и 3d - AO атома серы удовлетворяют этому условию. В соответствии с этим имеются данные, основанные на различных фактах, подтверждающие представление о том, что 3d - AO ( или гибридизованные 3d - АО) атома серы способны стабилизовать, а следовательно, и облегчать образование как свободнорадикальных, так и карбанионных систем. Так, установлено, что в длинной цепи полисульфида внутренние связи S - S могут быть легче разорваны гомолитическим путем, чем связи S - SB более коротких полисульфидных цепях. Возможно, что в более длинных радикалах R - ( S) x - S интенсивность делокализации неспаренного электрона больше. Интересно отметить также, что довольно высокая энергия диссоциации [ в среднем - 60 ккал / моль ( 251 21 - 103 Дж / моль) ] для связи S - SB дисульфиде может быть отчасти связана с делокализацией свободной пары электронов серы между двумя атомами серы. [3]
Соединения двухвалентной серы ( в отличие от соединений двухвалентного кислорода) легко окисляются. [4]
Соединения двухвалентной серы могут окисляться в жидкой фазе топлива. Жидкофазное окисление в таких сложных смесях, как моторные топлива, протекает последовательно, от более к менее реакционноспособному соединению. Реакционная способность соединений зависит в первую очередь от прочности химических связей. Мерой прочности химических связей является энергия, затрачиваемая на их разрыв. [5]
Органические соединения двухвалентной серы характеризуются сходным механизмом противозадир-ного действия. [6]
Органические соединения двухвалентной серы характеризуются сходным механизмом противозадир-ного действия, но различаются по своей активности. [7]
Органические соединения двухвалентной серы в значительных количествах содержатся в нефтепродуктах, сланцевых смолах и различных природных веществах и находят разнообразное применение в народном хозяйстве. Поэтому изучение подвижности атомов серы в молекулах этих соединений представляет не только теоретический, но и практический интерес. [8]
Из соединений двухвалентной серы сульфиды преобладают в нефтяных дистиллятах, выкипающих до 250 - 300 С. Нефтяные сульфиды на 75 - 95 % состоят из тиацикланов; ациклических структур всего 5 - 10 %, а ароматических сульфидов в продуктах прямой перегонки и того меньше. По-видимому, еще предстоит объяснить такую поразительную однотипность химического строения нефтяных сульфидов с точки зрения их происхождения в нефти. Из всех сернистых соединений неф-тей сульфиды исследованы наиболее полно. Во всяком случае, в настоящее время известен групповой химический состав сульфидов дистиллятов многих нефтей. [9]
Окисление соединения двухвалентной серы протекает сложно. По углеродным атомам молекулы оно идет по механизму радикально-цепной вырожденной реакции с образованием типичных для такого процесса кислородных функциональных групп. Атом же серы окисляется по ионному механизму, свободные валентные связи серы последовательно заполняются кислородом с образованием еульфоксидов, сульфонов, сульфоновых кислот и, наконец, сульфатов. Образуются и продукты взаимодействия соединений этой сложной системы. К наиболее глубокоокисленным сернистым соединениям в жидкой фазе следует отнести структуры, у которых свободная валентность атома серы полностью или почти полностью занята кислородом, например, сульфоновые кислоты, сульфонаты, сульфаты. По мере увеличения содержания кислорода в молекулах таких соединений их растворимость в углеводородной среде топлива падает. Наиболее глубоко окисленные структуры становятся растворимыми в воде и спирте. Однако в продуктах жидкофазного окисления соединений двухвалентной серы в моторном топливе образуются в основном соединения, хорошо растворимые в топливе. [10]
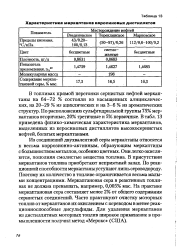 |
Характеристика меркаптанов керосиновых дистиллятов. [11] |
Из соединений двухвалентной серы меркаптаны относятся к весьма коррозионно-активным, образующим меркаптиды с большинством металлов, особенно цветных. Они легко окисляются, пополняя смолистые вещества топлива. В присутствии меркаптанов топлива приобретают неприятный запах. По реакционной способности меркаптаны уступают лишь сероводороду. Поэтому их количество в топливе ограничивается весьма малыми концентрациями. Меркаптановая сера в реактивных топливах не должна превышать, например, 0 005 % мае. На практике меркаптановая сера составляет менее 2 % от общего содержания сернистых соединений. Часто практикуют очистку моторных топлив от меркаптанов их окислением с переводом в менее реак-ционноспособные дисульфиды. [12]
Для определения двухвалентной серы сульфидных соединений и отличия ее от серы сульфино -, сульфоно - и сульфокислот можно применять следующий реактив [9]: в кипящую смесь 1 части воды и 2 частей глицерина вносят до насыщения свежеосажденный гидрат окиси кальция, добавляют также свежеосажденный гидрат окиси свинца или свинцовый глет, кипятят еще несколько минут, охлаждают, сливают с осадка и сохраняют раствор без доступа углекислоты. Можно рекомендовать также следующий способ [1]: несколько ми-крограммов слегка увлажненного вещества смешивают на платиновой пластинке с 4 - 10-кратным количеством смеси из 6 частей соды и 1 части хлорноватокислого калия. Смесь нагревают на пламени спиртовой горелки ( не на пламени светильного газа) до видимого окончания реакции, растворяют в воде и испытывают с хлористым барием на присутствие сульфата. [13]
Далеко идущая аналогия двухвалентной серы с кислородом методически проявляется в том, что получение сернистых соединений очень сходно с получением соответствующих им кислородных соединений. [14]
Различные органические соединения двухвалентной серы: сульфиды, дисульфиды, ксантогенаты и изотлурочиевъге соли действием хлора могут быть превращены в с. [15]
Страницы: 1 2 3 4