Взаимодействие - метан
Cтраница 1
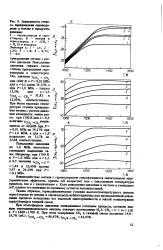 |
Зависимое степени превращения сероводорода и метана в продукты реакции. [1] |
Взаимодействие метана с сероводородом сопровождается значительным эндотермическим эффектом, причем ДЯ возрастает как с повышением температуры процесса, так и с увеличением а. Хотя повышение давления в системе и уменьшает дЯ, однако его величина no - прежнему остается положительной. [2]
Взаимодействие метана и аммиака в присутствии воздуха является сильно экзотермической реакцией. Это позволяет осуществлять процесс автотермично. [3]
Взаимодействие метана с водяным паром протекает с большой скоростью в отсутствие катализаторов при 1300 и выше. Для проведения процесса при более низкой температуре ( что по условиям равновесия возможно) требуется применение катализаторов. Активаторами никелевого катализатора служат окись магния, окись алюминия и др. Катализаторы наносят на огнеупоры. [4]
Взаимодействие метана и аммиака в присутствии воздуха является сильно экзотермической реакцией. Это позволяет осуществлять процесс автотермично. [5]
Взаимодействие метана с кислородом может протекать в нескольких направлениях. Направление взаимодействия метана с кислородом и характер получаемых при этом продуктов определяется содержанием кислорода в исходной метано-кислородной смеси, режимом процесса ( температурой, давлением, временем пребывания газа в зоне реакции), а также способом охлаждения продуктов реакции. При еще большем увеличении отяошения 02: СШ в исходной смеси в основном образуется СО и На. [6]
Взаимодействие метана с кислородом, при котором продуктами реакции являются СО и На, происходит с выделением тепла, что позволяет организовать данный процесс автотермично. Авто-термичность ( не связанная с внешним нагревом и с аккумуляцией тепла в зоне реакции) позволяет организовать процесс в сравнительно простой и дешевой аппаратуре при температурах порядка 900 С. При этом достигается высокий процент превращения метана. В аппаратуре этого типа можно без особых затруднений проводить процесс конверсии метана под давлением, при котором темпе - ратура процесса, во избежание недостаточной степени конверсии метана, должна быть еще выше. [7]
Взаимодействие метана с чистым кислородом в зависимости от содержания 02 в исходной смеси, температуры, давления, времени пребывания газов в реакционной зоне и способов охлаждения продуктов реакции может протекать в нескольких направлениях с образованием различных продуктов. [8]
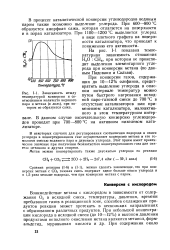 |
Зависимость между температурой конверсии и соотношением количеств водяного пара и метана ( в моль, при котором не образуется сажа. [9] |
Взаимодействие метана с кислородом в зависимости от содержания О2 в исходной смеси, температуры, давления, времени пребывания газов в реакционной зоне, способов охлаждения продуктов реакции может протекать в нескольких направлениях с образованием различных продуктов. [10]
Реакция взаимодействия метана с кислородом протекает стадийно и включает в себя совокупность элементарных реакций. [11]
Скорость взаимодействия метана с водяным паром ничтожна даже при 1500, в присутствии же катализаторов уже при 700 можно достигнуть равновесного выхода водорода. Для этого процесса предложено много катализаторов; наиболее активным, устойчивым к отравлению и достаточно дешевым оказался никель, нанесенный на пористый носитель. На этом катализаторе метан и другие углеводороды легко выделяют водород. Обычно в полученном таким способом газе содержатся примеси - сернистые соединения, СО и С02, кислород и вода. Все эти вещества отравляют железный катализатор синтеза аммиака. Поэтому водород подвергается тщательной очистке. Углекислый газ поглощают водой, а окись углерода медпо-аммначным раствором. Сернистые соединения адсорбируют активным углем, а воду удаляют с помощью осушителей. Такой способ можно использовать на заводах синтеза аммиака, где имеются холодильные установки для получения азота из воздуха. [12]
Начало взаимодействия метана с кислородом определяется периодом индукции - временем, необходимым для развития цепного процесса горения. [14]
При взаимодействии метана с водяным паром или углекислотой, добавляемыми в двукратном количестве ( против теоретически необходимого), выделение углерода не наблюдается ни на одном из исследованных нами никелевых катализаторов. [15]
Страницы: 1 2 3 4