Взаимодействие - метанол
Cтраница 3
С водой, спиртами, этиловым эфиром, бензолом, ацетоном, большей частью органических растворителей метиловый спирт смешивается в любых соотношениях. При взаимодействии метанола со щелочными металлами образуются алкоголяты, с кислотами - простые и сложные эфиры, с аммиаком - амины. При окислении метилового спирта вначале образуется формальдегид, затем - муравьиная кислота и, наконец, - двуокись углерода. [31]
Метил хлористый, СН3С1 - бесцветная, прозрачная летучая жидкость. Получают при взаимодействии метанола с хлорокисьго фосфора или треххлористым фосфором. [32]
Метил хлористый, СН3С1 - бесцетная, прозрачная летучая жидкость. Получают при взаимодействии метанола с хлорокисью фосфора или треххлористым фосфором. [33]
Температура кипения и парциальное давление паров трет-бутилметилового эфира таковы, что увеличение детонационной стойкости особенно влияет на октановое число. Синтез этого соединения осуществляют путем взаимодействия метанола и изобутена на кислых катализаторах с высокой селективностью. [34]
Рассмотрим, как практически используется идея о том, что вода является лучшей уходящей группой, чем гидроксид-ион. Выше было показано, что реакция взаимодействия метанола с бромид-ионом с образованием метилбромида пе происходит. Однако предположим, что мы имеем метанол и хотим превратить его в метилбромид. [35]
Первичные ТЭ и ТЭ многократной заливки по своему устройству различаются мало и их можно рассматривать вместе. Такой ТЭ состоит из анода и катода, между которыми находится раствор топлива и электролита. Такое устройство ТЭ возможно при условии малого взаимодействия или отсутствия взаимодействия метанола или формиат-ионов на катоде. В качестве катализаторов катода, на которых метанол и формиат-ионы практически не окисляются, могут быть активированный уголь, серебро, окислы металлов и фталоциаиины. Наиболее разработанным воздушным электродом является угольный пвдрофобизи-роваиный электрод. [36]
При образовании хлористого метила происходит совсем иное. Для молекулы органических соединений - а метанол, естественно, относится к ним - характерна атомная связь, никакой диссоциации и, следовательно, образования ионов ОН произойти не может. У спирта нельзя обнаружить никаких основных свойств, ведь эти свойства как раз обусловливаются присутствием гидроксильных ионов. Взаимодействие метанола с кислотой протекает медленно и не до конца, поскольку получающийся хлористый метил и вода реагируют между собой с образованием исходных соединений. Чем больше получается хлористого метила и воды, тем заметнее протекает обратная реакция. Наконец, наступает такой момент, когда в единицу времени распадается столько же молекул хлористого метила, сколько образуется вновь. Наступает состояние равновесия, определяющее конечный выход реакции. [37]
Синтез-газ является сырьем для нового, весьма перспективного способа производства кислородсодержащих продуктов, называемого оксо-нроцессом. Путем каталитического взаимодействия с олефипами Н2 и СО образуют альдегиды и первичные спирты с разветвленными цепями. Например, при взаимодействии метанола и СО может образоваться уксусная кислота, при присоединении СО к ацетилену акриловая кислота и ее производные. [38]
Синтез-газ является сырьем для нового, весьма перспективного способа производства кислородсодержащих продуктов, называемого оксо-процессом. Путем каталитического взаимодействия с олефинами Ш и СО образуют альдегиды и первичные спирты с разветвленными цепями. Например, при взаимодействии метанола и СО может образоваться уксусная кислота, при присоединении СО к ацетилену акриловая кислота и ее производные. [39]
Сшиванием двух молекул диалкилфенола, имеющего только одно реакционноспособное положение, реакцией с формальдегидом получают стабилизаторы класса бисфенолов для полимеров. Другой метод состоит в обработке фенола в присутствии кислоту диметоксиме-таном, ( МеО) 2СН2, который служит в данном случае и реагентом, и растворителем. Отщепляющийся в реакции метанол используют в синтезе диметоксиметана взаимодействием метанола с формальдегидом в присутствии кислоты. Пространственно затрудненные 2 6-диалкилфенолы, в отличие от 2 4-ди - алкилфенолов, с трудом взаимодействуют с формальдегидом в кислой среде, что объясняют стерическими затруднениями длят сопряжения гидроксигруппы с ароматической системой. [40]
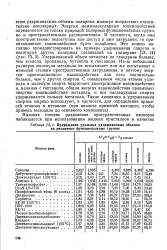 |
Приращение удельных удерживаемых объемов на различные функциональные группы. [41] |
Энергия межмолекулярных взаимодействий определяется не только природой полярных функциональных групп, но и пространственным расположением. В частности, когда они пространственно недоступны или доступ к ним затруднен, то ори-ентационное взаимодействие будет ослаблено. Из-за небольших размеров молекула метанола не испытывает или же испытывает в меньшей степени пространственные затруднения, и поэтому энергия оркентационного взаимодействия для него значительно больше, чем у других спиртов. С повышением числа атомов углерода в молекуле спирта возрастает дисперсионное взаимодействие и, начиная с гептанола, общая энергия взаимодействия превышает энергию взаимодействия метанола, и все последующие спирты удерживаются сильнее метанола. [42]
Страницы: 1 2 3