Взаимодействие - растворитель
Cтраница 2
Степень взаимодействия растворителя и компонентов определяет порядок выхода последних. [16]
 |
Зависимость теплоты гидратации ДЯгидр ( ккал / моль некоторых одновалентных катионов от их радиуса R ( А при t 25 С. [17] |
Интенсивность взаимодействия растворителя с ионом зависит от целого ряда факторов: к ним относится и энергия ионизации / атомов-ионообразователей. [18]
Продуктами взаимодействия растворителя с растворенными веществами являются сольваты, а процесс их образования называется с о л ь в а т а ц ней. Частным случаем сольватации является гидратация - взаимодействие растворенных веществ с водой, в результате которого образуются гидраты. Молекулы растворителя при сольватации ( гидратации) не разрушаются. Большинство сольватов, в том числе и гидраты, - малоустойчивые соединения. [19]
 |
Зависимость теплоты гидратации ДЯгидр ( ккал / г-ион некоторых одновалентных катионов. [20] |
Интенсивность взаимодействия растворителя с ионом зависит от целого ряда факторов; к ним относится и потенциал ионизации / атомов-ионообразователей. Поэтому с / связаны и теплоты, и энтропии сольватации. [21]
Процесс взаимодействия растворителя L с растворенным веществом KtAn сложен и приводит к образованию большого количества разнообразных частиц. [22]
При взаимодействии растворителя с растворенным веществом могут протекать реакции сольватации или сольволиза; важную роль играют также реакции десольватации, при которых происходит отделение молекул растворителя от молекул растворенного вещества. Соответствующие реакции, протекающие в воде, являются обычными реакциями гидратации и гидролиза; реакции дегидратации также являются общими и могут сопровождаться далеко идущими химическими изменениями. [23]
Изучая влияние взаимодействия растворителя с полимером на адсорбцию гибких макромолекул, он получил также [57] выражение для изменения удельной свободной энергии жидкой системы, когда Ms мест на поверхности заняты молекулами растворителя. [24]
 |
Эквивалентная электропроводность электролитов. [25] |
Важным показателем взаимодействия растворителей с ионами являются электродные потенциалы в растворах этих растворителей. Как известно, разность лотенциалов в различных растворителях определяется в первую очередь разностью диэлектрических проницаемостей и энергий сольватации. Так как диэлектрические проницаемости гидразина и воды мало различаются, то основной причиной различия электродных потенциалов в гидразине и воде может быть разность энергий сольватации. На значение электродного потенциала при взаимодействии гидразина с ионами металлов и водорода влияет образование комплексных ионов. [26]
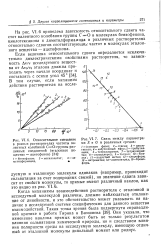 |
Относительное смещение в разных растворителях частоты валентных колебаний С0 - группы различных соединений ( эталонное вещество - ацетофенон.| Связь между параметрами S и G в различных средах. [27] |
Когда механизмы взаимодействия растворителя с эталонной и исследуемой молекулой различны, должно наблюдаться отклонение от линейности, и это обстоятельство может указывать на наличие в исследуемой системе специфических для данного вещества взаимодействий. Они указали, что изменение наклона прямых может быть не только результатом влияния сольватации химической природы, но и следствием влияния полярности среды на исследуемую молекулу, имеющую отличный от эталонной молекулы дипольный момент или радиус. [28]
Описанные варианты взаимодействия растворителя с дисперсной системой показывают каким образом, знея энергетические параметры взаимодействующих веществ, можно предсказать возможность образования новых ССЕ, преобразование старых ССЕ, образование СС, возможность разделения фаз. [29]
Однако при взаимодействии растворителя и растворенного вещества происходит не только ослабление кулоновских сил; галогенид и оксигалогенид по отношению к растворенному веществу часто выступают, как акцептор или донор галоидных ионов. При этом в процессе растворения образуются новые ионы. Они и вызывают самый живой интерес исследователей, работающих с неводными растворителями. [30]
Страницы: 1 2 3 4 5