Взаимодействие - углерод
Cтраница 1
Взаимодействие углерода с парами полония до 700 С не обнаружено. [1]
Взаимодействие углерода с а - или у-железом приводит к образованию твердых растворов по типу внедрения атомов углерода в свободные участки пространства кристаллич. В объемноцентрированной решетке а - Fe растворимость углерода весьма мала ( при комнатной темп-ре менее 0 008 %); этот раствор называется ферритом. В гранецеитрированной решетке у - Fe, существующей при высоких темл-рах, растворяется весь углерод стали ( предел растворимости углерода в у - Fe составляет 2 %), образующийся при этом раствор наз. Fe, то избыточные атомы углерода, не входящие в феррит, образуют с атомами железа хим. соединение - карбид железа ( Fe3C) - цементит. [2]
Взаимодействие углерода с кислородом, водяным паром и двуокисью углерода рассмотрено в ряде работ, например в [97, 98], применительно к горению и газификации твердых ископаемых топлив в различных условиях. [3]
Взаимодействие углерода и других компонентов с модификациями железа приводит к образованию различных структур. Твердый раствор углерода и других легирующих компонентов в у-железе называют аустенитом. Сталь, имеющую аустенитозую микроструктуру, называют аустенитной. Твердый раствор углерода и других легирующих компонентов в а и 5-железе называют сг-ферригом и 5-ферритом. Сталь, имеющую феррит-ную микроструктуру, называют ферритной. Механическую смесь феррита и цементита называют перлитом. Сталь, имеющую перлитную микроструктуру, называют перлитной. Если в стали увеличено содержание перлита, следовательно, увеличено и содержание углерода, что в свою очередь повышает прочность, снижая пластичность стали. [4]
Взаимодействие углерода с а - или у-железом приводит к образованию твердых растворов по типу внедрения атомов углерода Б свободные участки пространства кристаллич. В объемноцентрированпой решетке а - Fe растворимость углерода весьма мала ( при комнатной темп-ре менее 0 008 %); этот раствор называется ферритом. В гранецентрированной решетке у - Fe, существующей при высоких темп-рах, растворяется весь углерод стали ( предел растворимости углерода в у - Fe составляет 2 %), образующийся при этом раствор паз. Fe, то избыточные атомы углерода, не входящие в феррит, образуют с атомами железа хим. соединение - карбид железа ( Fe3C) - цементит. [5]
Взаимодействие углерода с углекислотой по реакции ( 319) практически для различных топлив начинается в интервале температур 700 - 1000 при отсутствии заметного количества свободного кислорода, причем скорость этой реакции по мере увеличения температуры непрерывно возрастает. [7]
Взаимодействие углерода с водяным паром сопровождается поглощением тепла. При высоких температурах разложение водяного пара происходит интенсивно, преимущественно по реакции ( 5) и зависит от реакционной способности топлива. [8]
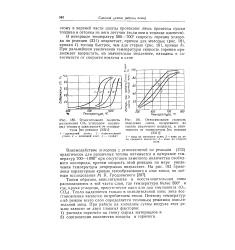 |
Относительная скорость окисления кокса, полученного из топлив различного возраста, в зависимости от температуры [ по реакции ( 231 ]. [9] |
Взаимодействие углерода с углекислотой по реакции ( 232) практически для различных топлив начинается в интервале температур 700 - 1000 при отсутствии заметного количества свободного кислорода, причем скорость этой реакции по мере увеличения температуры непрерывно возрастает. На рис. 182 приведены характерные кривые газообразования в слое кокса, по данным исследования М - К. [10]
Взаимодействие углерода с кислородом принято называть первичным процессом, а образующуюся при этом СО и СО2 - первичными продуктами. [11]
Схематически взаимодействие углерода коксового остатка с дутьем ( газом) можно разбить на три укрупненных этапа. Первым этапом является подвод дутья к раскаленному углероду. [12]
Процесс взаимодействия углерода с газообразными реагентами протекает как на внешней ( контурной), так и на внутренней поверхности макро - и микршор, доступных молекулам газообразного реагента. [13]
Продукт взаимодействия углерода с парами серы; имеет вид, прозрачной жидкости. Концентрация паров в воздухе в пределах 2 - 50 % образует взрывчатую смесь. Имеет эфирный запах, который со временем при хранении переходит в тяжелый запах. В зависимости от технологического процесса производства сероуглерод делится на три сорта: ректификат, полуректификат и сырец. [14]
Механизм взаимодействия углерода с парами кремнезема следует представлять как конденсацию паров кремнезема на поверхности угля и диффузию их внутрь по микропорам. Поэтому скорость образования карбида кремния зависит от крупности частиц угля, их микропористости, структуры, зольности и проч. [15]
Страницы: 1 2 3 4
