Взаимодействие - двуокись - углерод
Cтраница 2
Впервые алкилалюмоксановые соединения были упомянуты при взаимодействии двуокиси углерода с алюминийтриалкилом. [16]
Многие положения, высказанные исследователями по отношению к реакции взаимодействия двуокиси углерода с углеродом, применимы и к реакции обессеривания нефтяных коксов, также протекающей с образованием промежуточного комплекса. Действительно, в начальный момент обессеривания кинетическая энергия распавшихся углеводородных газов действует на сернистые соединения ( комплексы), вызывая понижение энергии активации их распада тем в большей степени, чем выше скорость нагрева нефтяного кокса. [17]
Карбонат-ионы - по образованию белого осадка карбоната бария при взаимодействии двуокиси углерода, выделяющейся из подкисленного раствора, с баритовой водой. [18]
Из двух реакций, составляющих процесс восстановления, наиболее медленной является взаимодействие двуокиси углерода с сажей. Поэтому скорость процесса восстановления окиси железа определяется скоростью взаимодействия двуокиси углерода с сажей. [19]
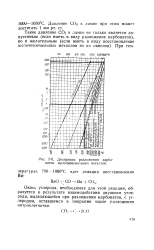 |
Диаграмма разложения карбонатов щелочноземельных металлов. [20] |
Окись углерода, необходимая для этой реакции, образуется в результате взаимодействия двуокиси углерода, выделяющейся при разложении карбонатов, с углеродом, оставшимся в покрытии после разложения нитроклетчатки. [21]
Сказанное также дает основание полагать, что прямое восстановление в вакууме окислов различных металлов и их соединений нередко лимитируется одной и той же реакцией, а именно взаимодействием двуокиси углерода с углем. [22]
Важность этого вопроса заключается в том, что хлорофилл имеет две азотно-магниевые связи. Взаимодействие двуокиси углерода с хлорофиллом будет рассмотрено в главе XVI. Один моль твердого или коллоидального хлорофилла способен к абсорбции двух молей двуокиси углерода. [23]
Взаимодействие двуокиси углерода с ним происходит на его поверхности, а поэтому с ее увеличением химический процесс ускоряется. [24]
Получают взаимодействием двуокиси углерода и фенолята натрия при температуре около 200 С под давлением. Са-лициловокислый натрий затем разлагают соляной кислотой; получаемую салициловую кислоту очищают возгонкой или перекристаллизацией. [25]
Аммоний углекислый 40 % - ный - желтоватая жидкость с запахом аммиака. Получают взаимодействием двуокиси углерода с водным раствором аммиака. [26]
Особенно легко осуществляется введение карбоксильной группы н фс-лолы. Реакция проводится при нагревании путем взаимодействия двуокиси углерода с сухим фенолятом под давлением. [27]
Экспериментальные исследования этих проблем, в частности выяснение роли сульфатов в стекле, особенно сложны. Мы значительно больше знаем о взаимодействии двуокиси углерода с расплавом и о том, почему остатки карбонатов сохраняются в стекле. Уэйл 69 изучил эти проблемы, применяя высокие давления двуокиси углерода при реакциях, протекающих в обоих направлениях. Увеличение давления и уменьшение температуры сдвигает равновесие в сторону образования карбоната. [28]
При сгорании угля в нижней части генератора образуется газовая смесь, состоящая из азота, двуокиси углерода и водяных паров. В верхней части камеры в результате взаимодействия двуокиси углерода и водяных паров с раскаленным углем образуется окись углерода и водород. Газы, выходящие из генератора, поступают через фильтр на очистку. [29]
Из двух реакций, составляющих процесс восстановления, наиболее медленной является взаимодействие двуокиси углерода с сажей. Поэтому скорость процесса восстановления окиси железа определяется скоростью взаимодействия двуокиси углерода с сажей. [30]
Страницы: 1 2 3