Ориентационное индукционное взаимодействие
Cтраница 1
Ориентационные и индукционные взаимодействия составляют, однако, лишь часть межмолекулярного ван-дер-ваальсового притяжения. [1]
Ориентационное и индукционное взаимодействия представляют собой электростатическую компоненту адсорбционных сил. Ориентационное взаимодействие играет основную роль для нейтральных молекул. [2]
 |
Схематическое изобра. [3] |
Наряду с ориентационным и индукционным взаимодействием существует третий вид слабого взаимодействия, который объясняется перемещением электронов в атоме или в молекуле, вызывающим возникновение маленьких мгновенных диполей в молекулах и атомах. С этим связана возможность перевода веществ, состоящих из неполярных молекул ( водород, азот, кислород, метан и пр. [4]
Наряду с ориентационным и индукционным взаимодействием существует еще один вид взаимодействия, который объясняется перемещением электронов в атоме или в молекуле, вызывающим возникновение мгновенных диполей в молекулах и атомах. С этим связана возможность перевода веществ, состоящих из неполярных молекул ( водород, азот, кислород, метан и др.) и атомов ( благородные газы), в конденсированное состояние. [5]
 |
Схематическое изображение ориентационного ( а, индукционного ( б и дисперсионного ( в взаимодействия между молекулами. [6] |
Наряду с ориентационным и индукционным взаимодействием существует еще один вид взаимодействия между молекулами, который объясняется перемещением электронов в атоме или в молекуле, вызывающим возникновение мгновенных диполей в молекулах и атомах. [7]
Представление об ориентационном и индукционном взаимодействии позволило понять причины взаимного притяжения молекул в том случае, если все молекулы или часть их являются полярными. Но опыт показывает, что силы Ван-дер - Ваальса действуют между частицами и в тех случаях, когда они неиолярны. Таковы, например, атомы инертных газов, электронные оболочки которых обладают сферической симметрией. С другой стороны, выяснилось, что даже в случае полярных молекул ориентационное и индукционное взаимодействие составляют лишь часть наблюдаемого на опыте ван-дер-ваальсова взаимодействия. [8]
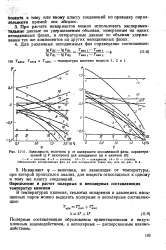 |
Зависимость величины ср от полярности неподвижной фазы, характеризуемой Ig V ( изопрена для алкадиенов ( а и алкинов ( б. [9] |
Полярные составляющие обусловлены ориентационным и индукционным взаимодействием, а неполярные - дисперсионным взаимодействием. [10]
Согласно современным теориям адсорбция обусловливается дисперсионным, ориентационным и индукционным взаимодействием. [11]
 |
Дипольные моменты молекул. а - схема молекулы воды. б - дипольный момент молекулы водыи, -. 1 84 D. [12] |
Между полярными молекулами, кроме дисперсионного, существует еще ориентационное и индукционное взаимодействия. [13]
При физической адсорбции на поверхности ионных кристаллов основную роль играют ориентационное и индукционное взаимодействия, а при адсорбции на угле и других подобных материалах процесс определяется дисперсионным взаимодействием. [14]
При физической адсорбции на поверхности ионных кристаллов основную роль играют ориентационное и индукционное взаимодействия, а при адсорбции на угле и других подобных материалах процесс определяется дисперсионным взаимодействием. [15]
Страницы: 1 2 3