Донорно-акцеп-торное взаимодействие
Cтраница 1
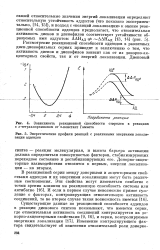 |
Энергетические профили реакций с различными энергиями локализации аддендов. [1] |
Донорно-акцеп-торные взаимодействия относятся к первым, энергии локализации - ко вторым. [2]
Подобное донорно-акцеп-торное взаимодействие приводит к образованию связей различной прочности на границе раздела фаз. Несколько утрируя, можно сказать, что прочность всех физических тел, а не только адгезионных соединений, определяется взаимодействием электронов. [3]
 |
Орбитали при транс - ( 1 и цис-элиминировании ( 2. [4] |
Оэщий вызод о благоприятном донорно-акцеп-торном взаимодействии при существенном перекрывании комбинирующихся орбиталей приводит к интересному заключению, касающемуся стереохимии молекул, подвергающихся замещению в винилогичных положениях. [5]
Таким образом, температурные опыты не противоречат донорно-акцеп-торному взаимодействию, как причине наблюдаемых явлений. [6]
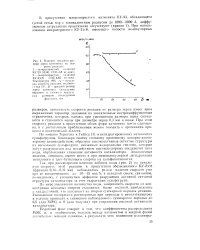 |
Влияние среднего размера зерна катионита на скорость реакции. [7] |
По мнению Торнтона и Гейтса [ 3.1 в негидратированных катионитах сульфогруипы, благодаря своему сильному протонному донорно-акцеп-торному взаимодействию, образуют высокоактивные сетчатые структуры, из нескольких сульфогрупп, связанных водородными связями, которые могут разрушаться под воздействием высокополярных соединений типа воды, обусловливая снижение активности катализатора. Аналогичные явления, очевидно, имеют место и при межмолекулярной дегидратации, метилового и ту т-бутилового спиртов на сульфокатионитах. [8]
В основном дело сводится к тому, что элементы Si, P, S, C1 способны к особому донорно-акцеп-торному взаимодействию и образованию гибридных волновых функций, отвечающих внешним, валентным облакам, включающим в себя З - состоя-ния. Это влечет за собой и способность фосфора, серы и хлора образовывать молекулы PF5, SFe, C1F3 также с участием Зс ( - состояний ВЯ-СБЯЗИ. [9]
Так, в работах Соколова ( см., например, [3]) было показано, что к такому результату может приводить донорно-акцеп-торное взаимодействие реагентов с АЦ. [10]
Такое перекрывание, по-видимому, благоприятствует образованию положительных ионов, особенно в случае ксенона. Донорно-акцеп-торное взаимодействие нельзя объяснить на основании разностей электроотрицательностей [103], так как маловероятно, чтобы молекулы СН4, С2Н6 и О2 играли роль доноров электронов. Например, кислород имеет сродство к электрону около б в, а работа выхода ртути равна 4 5 в, так что с точки зрения электроотрицательностей внешняя сторона физически адсорбированного на ртути слоя кислорода должна быть заряжена отрицательно. [11]
Аналогичная схема, возможно, имеет место и при взаимодействии диаминов с дикарбоновыми кислотами, хотя это не подтверждено литературными данными. Отмечают [7], что донорно-акцеп-торное взаимодействие способствует созданию такой ориентации мономеров в системе, которая благоприятствует протеканию реакции, снижая величину предэкспоненциального множителя и энергию активации. Образование КПЗ зафиксировано для ряда систем: галогенангидри-ды - третичные и первичные амины [7; 16-18], пиромеллитовый диан-гидрид - диамины [19] и др. В ряде случаев удалось выделить КПЗ как индивидуальные химические соединения. КПЗ - энергетически неустойчивая система. Под влиянием внешних факторов происходит полный перенос электрона от донора к акцептору и образуется о-комплекс. Обе стадии ( образование КПЗ и ст-комплекса) являются равновесными, имеют высокую скорость и низкую энергию активации. [12]
Для количественного изучения некоторых типов координации, обусловленных донорно-акцеп-торным взаимодействием, оказалось удобным измерять распределение одного из компонентов, обычно донора, между такой жидкой фазой, в которой только этот компонент заметно растворим, и жидкой фазой, которая содержит как донор и акцептор, так и комплекс в целом. Этот метод Уинстейн и Лукас [6] использовали при изучении координации ионов серебра с ненасыщенными соединениями в водной среде. [13]
Неподеленные пары электронов играют важную роль в проявлении химических свойств соединений. В частности, они ответственны за способность соединений вступать в донорно-акцеп-торное взаимодействие. [14]
Со многими ионами молекулы воды взаимодействуют специфически. Кроме сил обычного для полярных растворителей ион-дипольного взаимодействия имеют место донорно-акцеп-торные взаимодействия за счет неподеленных электронных пар воды и водородные связи. [15]
Страницы: 1 2