Динитрофенилирование
Cтраница 1
Динитрофенилирование проводят в среде триметиламина по методу, приведенному в П 95, но в отличие от этого метода реакционную смесь не экстрагируют, а пропускают через колонку, заполненную зеролитом - Н в СГ-форме, после чего промывают небольшим количеством воды. При этом непрореагировавшая часть пептида удаляется. ДНФ-пептид десорбируют небольшим количеством ледяной уксусной кислоты. В элюат через колонку проходят свободные аминокислоты. [1]
Реакция динитрофенилирования шла количественно в диокса-новом растворе при нагревании в течение 5 - 10 мин. [2]
Реакция динитрофенилирования пептидов и белков с последующим кислым гидролизом широко используется для установления N-концевых аминокислот. [3]
РСак и динитрофенилирование, эту реакцию рекомендуется проводить в том случае, когда смесь аминокислот из-за наличия примесей нельзя непосредственно анализировать методом ХТС: ФТГ-аминокислоты часто легче перевести в хроматографируемую форму, чем свободные аминокислоты. [4]
Как и динитрофенилирование, эту реакцию рекомендуется проводить в том случае, когда смесь аминокислот из-за наличия примесей нельзя непосредственно анализировать методом ХТС: ФТГ-аминокислоты часто легче перевести в хроматографируемую форму, чем свободные аминокислоты. [5]
Различные методы динитрофенилирования отличаются условиями проведения реакции и аппаратурным оформлением. [6]
Значение реакции динитрофенилирования состоит прежде всего в том, что она приводит к количественному образованию кристаллических соединений желтого цвета, которые легко отделяются при хроматографировании и могут быть количественно определены спектрофотометрическим методом. Кроме того, связь ДНФ - аминокислота в продуктах реакции динитрофенилирования не гидролизуется кислотой, что позволяет использовать эту реакцию для определения N-концевых аминокислот в белках ( см. гл. [7]
Различные методы динитрофенилирования отличаются условиями проведения реакции и аппаратурным оформлением. [8]
Для определения аминов проводили их динитрофенилирование и динитро бензоилирование, продукты реакции вводили в реакцию Яновского. Сине-фио летовый раствор спектрофотометрировали при тах 4004 - 560 им ( для различ. [9]
Нами были найдены условия количественного протекания реакции динитрофенилирования и динитробензоилирования и реакции Яновского для аминов различного строения: ароматических первичных моноаминов, диаминов и вторичных аминов с различными функциональными заместителями, а также жирных первичных и вторичных аминов, некоторых гетероциклических аминов ряда пирролидина, пиразола, пирона, фурфурола и пиридина. [10]
Анализ состоит из следующих стадий: 1) динитрофенилирование, 2) удаление избытка реагента, 3) гидролиз ДНФ-производного, 4) растворение ДНФ-аминокислот. [11]
По более усовершенствованной методике отщепившиеся аминокислоты превращают путем динитрофенилирования в соответствующие ДНФ-производные, а гидразиды аминокислот - в ди - ДНФ-лроизводные. Например, 1 мкмоль белка гидролизуют примерно с 1 г безводного гидразина ( 99 - 100 %) при 100 в течение 5 - 10 час. Смесь осторожно упаривают в вакууме над концентрированной серной кислотой, остаток растворяют в 15 мл 2 % - ного раствора бикарбоната Na или 0 2 / И фосфатного буфера, рН 8, и добавляют раствор 0 3 мл ФДНБ в 30 мл этанола. Реакционную смесь встряхивают в течение 2 час в темноте при комнатной температуре, добавляют 45 мл воды и раствор подкисляют разведенной соляной кислотой. ДНФ-производные экстрагируют этилацетатом, а затем из этилацетата кислые ДНФ-производные извлекают 2 % - ным раствором бикарбоната. Производные С-концевых аминокислот, а также глутаминовой и аспарагиновой кислот осаждают из водного раствора при подкислении разбавленной кислотой, снова экстрагируют этилацетатом и хроматографируют на силикагеле. [12]
В основу определения замещенных гидразинов положена реакция их динит-робензоилирования и динитрофенилирования. [13]
ДНФ-цистеиновая кислота в отличие от ДНФ-цистина устойчива к гидролизу, поэтому перед динитрофенилированием выгодно цистино-вые пептиды окислять надмуравьипой кислотой. [14]
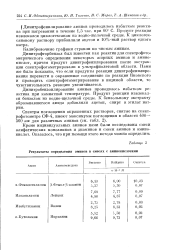 |
Результаты определения аминов в смесях с аминокислотами. [15] |
Страницы: 1 2