Динитрофенилирование
Cтраница 2
Динитрофторбензол был известен как реактив для спектрофото-метрического определения некоторых жирных аминов и аминокислот, причем продукт динитрофенилирования после экстракции спектрофотометрировали в ультрафиолетовой области. Нами же было показано, что если продукты реакции динитрофенилирования перевести в окрашенное соединение по реакции Яновского и проводить спектрофотометрирование в видимой области, то чувствительность реакции увеличивается. [16]
Эту методику применяли для разделения аминокислот и пептидов, образующихся при действии проназы на нативную и модифицированную ( путем окисления, динитрофенилирования и окисленияЧ - динитрофенилирование) рибонуклеазу 21 ]; В первом варианте 2 4-динитроанилин вымывался вблизи ДНФ-ала-нина. Когда же в смеситель / вместо - гептана вводили смесь толуол - - гептан, 2 4-динитроанилин начинал элюироваться в меньшем объеме, а положение остальных пиков осталось прежним. Однако все эти предосторожности излишни, поскольку реагент и побочные продукты реакции вымываются раньше ДНФ-аминокислот. [17]
В отличие от определения N-концевых групп в пептидных цепочках, для которого мы располагаем удобными и широко распространенными химическими методами идентификации, например динитрофенилирование или реакция с фенилизотиоцианатом, для работы с С-конневыми аминокислотами в пептидах и белках лучше всего зарекомендовал себя ферментативный ( карбоксипептидазный) метод, который имеет, однако, некоторые ограничения. Этот метод нельзя, например, применять для нерастворимых белков ( кератин и фиброин), и, кроме того, па течение реакции наряду с концевой аминокислотой оказывает влияние также предпоследняя аминокислота. Из химических методов для определения карбоксильных групп был разработан тиогидантоиновый метод, который дает относительно низкие выходы, и, кроме того, метод восстановления, сведения о котором, встречающиеся в литературе, весьма противоречивы. Нам кажется, что довольно хорошим методом, дополняющим результаты, полученные карбоксипептидазным методом, будет гидразинолиз, совместно с доказательством и определением С-концевой аминокислоты в виде динитрофенил-нроизводного. Остальные методы, приведенные в табл. 84, применяются довольно редко. [18]
Эту методику применяли для разделения аминокислот и пептидов, образующихся при действии проназы на нативную и модифицированную ( путем окисления, динитрофенилирования и окисленияЧ - динитрофенилирование) рибонуклеазу 21 ]; В первом варианте 2 4-динитроанилин вымывался вблизи ДНФ-ала-нина. Когда же в смеситель / вместо - гептана вводили смесь толуол - - гептан, 2 4-динитроанилин начинал элюироваться в меньшем объеме, а положение остальных пиков осталось прежним. Однако все эти предосторожности излишни, поскольку реагент и побочные продукты реакции вымываются раньше ДНФ-аминокислот. [19]
Такое избирательное расщепление фосфоамидной связи в нуклео-тидил - ( 5 - - N) - пептидах гидроксиламином ( рН 4 5) было использовано для определения в них N-концевой аминокислоты; фиксирование освободившегося пептида осуществлялось динитрофенилированием. [20]
Именно поэтому классический метод Сэнгера явился значительным достижением в белковой химии; его принцип заключается в следующем. В результате происходит динитрофенилирование N-концевых аминогрупп, а также некоторых реакционноспособных боковых цепей, имеющих следующие группы: e - NH2, фенольные - ОН, имида-зольные - NH и - SH. После этого динитрофенильные ( ДНФ) производные белков или пептидов подвергают кислотному гидролизу и экстрагируют эфиром а - ДНФ-аминокислоты, занимавшие в белке или пептиде N-концевое положение. После экстракции в гидролизате остаются только водорастворимые ДНФ-аргинин и ДНФ-лизин. [21]
Наибольшее применение для определения N-концевых остатков в настоящее время находит разработанный в 1963 г. В. Как и метод динитрофенилирования, он основан на введении в аминогруппы белка метки, ие удаляющейся при последующем гидролизе. [22]
ДНФ-производные пептидов низкого молекулярного веса могут быть экстрагированы из реакционной смеси не содержащим перекисей эфиром; ДНФ-производные пептидов более высокого молекулярного веса можно экстрагировать этилацетатом или н-бутано-лом после извлечения динитрофенола из смеси эфиром. Сэнджер и Томпсон [12] описали методику динитрофенилирования пептидов, позволяющую непосредственно хроматографировать ДНФ-производные. Данная методика исключает применение солевых растворов. Пептид элюируют с полоски бумаги ( ватман № 3) и после высушивания растворяют в 0 1 мл 1 % - ного триметиламина. Добавляют этанол ( 0 2 мл) и ДНФБ ( 0 01 мл), и через 2 час избыток ДНФБ трижды экстрагируют эфиром. Гидролиз удобно проводить в толстостенной капиллярной трубке. Гидролизах разводят 2 объемами воды, и ДНФ-аминокислоты экстрагируют трижды эфиром. Если в составе пептида ( но не в N-концевом положении) имеются тирозин и лизин, то они превращаются в водорастворимые производные; О-ДНФ-тирозин и е - ДНФ-лизин. Гисхидин медленно превращается в ши - ДНФ-гистидин, который также растворим в воде. К другим производным, не экстрагирующимся из кислых водных растворов, относятся ДНФ-цистеиновая кислота, ди - ДНФ-гисхн-дин, S-ДНФ-цистеин и сс - ДНФ-аргинин. [23]
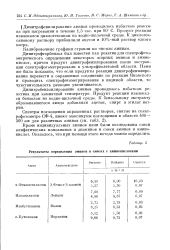 |
Результаты определения аминов в смесях с аминокислотами. [24] |
Динитрофторбензол был известен как реактив для спектрофото-метрического определения некоторых жирных аминов и аминокислот, причем продукт динитрофенилирования после экстракции спектрофотометрировали в ультрафиолетовой области. Нами же было показано, что если продукты реакции динитрофенилирования перевести в окрашенное соединение по реакции Яновского и проводить спектрофотометрирование в видимой области, то чувствительность реакции увеличивается. [25]
Значение реакции динитрофенилирования состоит прежде всего в том, что она приводит к количественному образованию кристаллических соединений желтого цвета, которые легко отделяются при хроматографировании и могут быть количественно определены спектрофотометрическим методом. Кроме того, связь ДНФ - аминокислота в продуктах реакции динитрофенилирования не гидролизуется кислотой, что позволяет использовать эту реакцию для определения N-концевых аминокислот в белках ( см. гл. [26]
ДНФ-производное орнитина можно получить аналогичным образом. N-ДНФ-Гис очень быстро образуется при добавлении небольшого количества ДНФБ, а динитрофенилирование ацетильного производного дает М - ДНФ-Гис. [27]
Важное значение для их анализа имеют р-ции с 1-диметиламино - 5-нафталинсульфо-хлоридом ( дансилирование) и 1-фтор - 2 4-динитробензолом ( динитрофенилирование); получаемые при этом продукты гидролизуются до стабильного производного N-концевой аминокислоты, к-рое идентифицируют хроматографически. [28]
III), методом определения N-концевых аминокислот может быть динитрофторбензольный метод Сэнджера. После динитрофенилирования и гидролиза динитро-фенилпроизводного белка ( ДНФ-производное), продукты реакции - ДНФ-аминокислоты - сорбируют при рН 7 - 6 на анионо-обменной смоле, тогда как свободные аминокислоты остаются в растворе. Это обусловлено тем, что ДНФ-аминокислоты при этом рН являются анионами, тогда как свободные аминокислоты - цвиттерионами или катионами, не сорбируемыми аниони-том. Окрашенные производные элюируют затем со смолы кислотой, разделяют при помощи двумерной бумажной хроматографии, идентифицируют с помощью соответствующих свидетелей и рассчитывают количество молей ДНФ-аминокислот на 1 моль белка. Это позволяет найти число свободных N-терминальных групп и, следовательно, число полипептидных цепей в белке. N-концевые аминокислоты могут быть определены и в виде фе-нилтиогидантоиновых производных или свободных кислот из них по методу Эдмана. [29]
Гидролиз цитохрома с химотрипсином дал тринадцать больших пептидов, которые были разделены хроматографией на ионообменных смолах и очищены далее при помощи электрофореза и хроматографии на бумаге. Аминокислотная последовательность пептидов была установлена при помощи химических и ферментативных методов. Химические методы включали динитрофенилирование по Сэнджеру и деградацию по Эд-ману для идентификации N-концевых аминокислот, ферментативные - гидролиз лейцинаминопептидазой для определения N-концевых и карб-оксипептидазой А для определения С-концевых аминокислот; оба фермента использовались также для определения коротких аминокислотных последовательностей. [30]
Страницы: 1 2