Высшая алюминийтриалкила
Cтраница 2
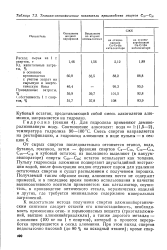 |
Технико-экономические показатели производства спиртов С10 - С20. [16] |
К недостаткам метода получения спиртов алюминийорганиче-ским синтезом следует отнести его многостадийность, необходимость применения огне - и взрывоопасных веществ ( триэтилалюми-ний, высшие алюминийтриалкилы), а также дорогого металла - алюминия ( 100 кг на 1 т спиртов), который в процессе переработки превращается в оксид алюминия. [17]
К недостаткам метода получения спиртов алюминийорганиче-ским синтезом следует отнести его многостадийность, неебходи-мость применения огне - и взрывоопасных веществ ( триэтилалюми-ний, высшие алюминийтриалкилы), а также дорогого металла - алюминия ( 100 - 120 кг на 1 т спиртов), который в процессе переработки превращается в окись алюминия-отход производства. Достоинствами метода являются низкая стоимость и доступность этилена, а также получение в результате синтеза высококачественных первичных спиртов, которые можно применять в производстве пластификаторов и синтетических моющих средств. [18]
Большое значение имеют и высшие алюминийтриалкилы - как исходное сырье для получения первичных высших спиртов. Высшими алюминийтриалкилами считаются соединения, содержащие у атома алюминия алкильные группы С6 и выше. [19]
У три-н-гексилалюми-ния ( и, может быть, у не исследованного до сих пор три-н-пентилалюми-ния) комплексообразова-ние с фтористым натрием внезапно прекращается. Фторид полностью нерастворим в высших алюминийтриалкилах. [20]
Сущность процесса заключается в следующем. Вначале при взаимодействии триэтилалюминия с этиленом идет реакция роста цепи; в результате получаются высшие алюминийтриалкилы с прямой алкильной цепью. Их затем окисляют воздухом с образованием н-алкилалкоголятов алюминия, гидролизом которых получают в итоге смесь высших первичных спиртов с четным числом атомов С в молекуле. Получаемые спирты представляют собой в основном смесь спиртов Се - Ci8; длину углеводородного радикала можно регулировать, изменяя на стадии полимеризации соотношение между триэтилалюминием и этиленом. [21]
Как уже указывалось, самопроизвольное отщепление олефина от триалкил-алюминия ( первая стадия реакции - некатализируемое вытеснение) имеет больший температурный коэффициент, чем реакция достройки, поэтому при температурах около 200 высшие алюминийтриалкилы практически больше не образуются, а получаются наряду с триэтилалюминием и олефины. Названная область температур является уже оптимальной для каталитической димеризации а-олефинов ( см. стр. Все же такой ход реакции возможен. Он даже был, как уже описано ранее [7, 8, 10], исходным пунктом для открытия реакций достройки и вытеснения. Чтобы полиме-ризовать этим способом этилен, в принципе не требуется ничего, кроме нагревания его примерно до 200 при повышенном давлении в автоклаве с триалкилалюминием, его эфиратами, алюмогидридом лития или с алюмотетраэтиллитием ( в эфире), Этот вид каталитической полимеризации этилена здесь подробно не описывается, так как он, хотя и давно известен, еще далеко не совершенен. К этому следует вернуться после окончания ведущихся исследований. [22]
Как уже указывалось, самопроизвольное отщепление олефина от триалкил-алюминия ( первая стадия реакции - некатализируемое вытеснение) имеет больший температурный коэффициент, чем реакция достройки, поэтому при температурах около 200 высшие алюминийтриалкилы практически больше не образуются, а получаются наряду с триэтилалюминием и олефины. Названная область температур является уже оптимальной для каталитической димеризации а-олефинов ( см. стр. Все же такой ход реакции возможен. Он даже был, как уже описано ранее [7, 8, 10], исходным пунктом для открытия реакций достройки и вытеснения. Этот вид каталитической полимеризации этилена здесь подробно не описывается, так как он, хотя и давно известен, еще далеко не совершенен. К этому следует вернуться после окончания ведущихся исследований. [23]
Обнаружить комплексы двух низших алюминийтриалкилов было легко, так как от исходных веществ эти новые соединения отличаются рядом характерных свойств. По самопроизвольной кристаллизации или же по образованию второй жидкой фазы они могут быть признаны особыми новыми веществами. При переходе к высшим алюминийтриалкилам такая возможность исчезает. Комплексные соединения часто не кристаллизуются, они почти всегда растворимы в алюминийтриалкилах и поэтому двух жидких фаз не образуется. Если установлено, что хлористый калий в триэтилалюминии подчиняется этому условию, а бромистый калий нерастворим даже в виде следов, то это явление не следует объяснять тем, что хлорид как таковой специфически растворим, а бромид нерастворим. Необходимо допустить в первом случае образование нового вещества, поскольку бромиды щелочных металлов в органических растворителях более растворимы, чем хлориды щелочных металлов. Еще более убедительно то, что такой галогенид щелочного металла, как хлористый рубидий, в одном из двух алюминийтриалкилов, алкильные группы которых по числу атомов С близки между собой, а именно в три-н-бутилалюминии, растворяется до молярного соотношения 1: 1, а во втором - три-н-гексилалюми-нии - совсем нерастворим. В первом случае комплекс стабилен, во втором - комплекс неустойчив. [24]
Обнаружить комплексы двух низших алюминиитриалкилов было легко, так как от исходных веществ эти новые соединения отличаются рядом характерных свойств. По самопроизвольной кристаллизации или же по образованию второй жидкой фазы они могут быть признаны особыми новыми веществами. При переходе к высшим алюминийтриалкилам такая возможность исчезает. Комплексные соединения часто не кристаллизуются, они почти всегда растворимы в алюминийтриалкилах и поэтому двух жидких фаз не образуется. Несмотря на это, о комплексе-образовании можно уверенно судить по тому, что галогениды щелочных металлов растворяются в молярных соотношениях, не превышающих соотношения 1: 1, Если установлено, что хлористый калий в трнэтилалгоминнн подчиняется этому условию, а бромистый калий нерастворим даже в виде следов, то это явление не следует объяснять тем, что хлорид как таковой специфически растворим, а бромид нерастворим. Необходимо допустить в первом случае образование нового вещества, поскольку бромиды щелочных металлов в органических растворителях более растворимы, чем хлориды щелочных металлов. Еще более убедительно то, что такой галогенид щелочного металла, как хлористый рубидий, в одном из двух алюминиитриалкилов, алкильные группы которых по числу атомов С близки между собой, а именно в три-н-бутилалюминии, растворяется до молярного соотношения 1: 1, а во втором - три-н-гекснлалюми-нии - совсем нерастворим. В первом случае комплекс стабилен, во втором - комплекс неустойчив. [25]
Известны отдельные случаи, когда соединение 1: 1 в присутствии избытка триалкилалюминия выделяется как несмешивающаяся новая фаза с определенным составом. При полной растворимости комплекса в триялкилалюмииии обнаружить комплекс 1: 2 непосредственным наблюдением очень трудно. Это относится особенно к комплексам фторидов щелочных металлов с высшими алюминийтриалкилами. Для NaCN и KCN соответствующие опыты еще не проведены. [26]
Известны отдельные случаи, когда соединение 1: 1 в присутствии избытка триалкилалюминия выделяется как несмешивающаяся новая фаза с определенным составом. При полной растворимости комплекса в триалкилалюминии обнаружить комплекс 1: 2 непосредственным наблюдением очень трудно. Это относится особенно к комплексам фторидов щелочных металлов с высшими алюминийтриалкилами. Для NaCN и KCN соответствующие опыты еще не проведены. [27]
Триметилалю-миний не способен к ступенчатому присоединению этилена, так как первый этап процесса присоединения ( а. В присутствии триметил-алюминия скорость присоединения других алюминийтриалкилов к этилену уменьшается. Обсуждаются возможные объяснения этого явления. Трипропилалюминий легко присоединяет этилен, превращаясь в высшие алюминийтриалкилы с нечетным числом атомов углерода. [28]
Триметилалю-миний не способен к ступенчатому присоединению этилена, так как первый этап процесса присоединения ( alCHs - AlCsH. В присутствии триметил-алюминия скорость присоединения других алюминийтриалкилов к этилену уменьшается. Обсуждаются возможные объяснения этого явления. Трипропилалюминий легко присоединяет этилен, превращаясь в высшие алюминийтриалкилы с нечетным числом атомов углерода. [29]
Можно вести процесс с сесквихлоридом, не выделяя первую стадию в самостоятельную, однако в этом случае на единицу образующегося триалкилалюминия приходится большое количество твердой соли, что приводит к образованию густой, трудно перемешиваемой реакционной массы. Для того чтобы реакционная масса не затвердевала и оставалась легко подвижной, целесообразно вести реакцию в среде растворителя. Желательно выбирать растворители, значительно отличающиеся по температуре кипения от получаемых алюминийтриалкилов. С низкокипящими растворителями приходится работать под давлением. Следует избегать избытка фтористого натрия, который дает с алюминийтриалкилами прочные комплексные соединения. Для связывания избытка фтористого натрия рекомендуется добавлять фтористый алюминий, образующий с фтористым натрием криолит. Для этого рекомендуют откачивать образующиеся пары алюминийтриалкилов при помощи мощных вакуум-насосов. Чем длиннее цепь алкильного радикала в триалкил-алюминии, тем более глубокий вакуум необходим. Высшие алюминийтриалкилы получают при 230 - 250 и давлении 1 мм. Вместо отгонки в вакууме может применяться отгонка в токе перегретых паров инертного растворителя, например пентана или бензола. [30]
Страницы: 1 2