Фталевый ангидрид
Cтраница 1
Фталевый ангидрид применяется в производстве алкидных смол, входит в состав красок и лаков. [1]
Фталевый ангидрид горюч и представляет умеренную пожарную опасность. Его токсичность относительно низка по сравнению с другими промышленными кислотными ангидридами, но он является раздражителем для кожи, глаз и верхних дыхательных путей. [2]
Фталевый ангидрид должен храниться в прохладном, хорошо проветриваемом помещении вдали от открытого огня и окислителей. В помещениях, где он используется, необходима хорошая местная и обшая вентиляция. Во многих процессах фталевый ангидрид используется не в твердом виде, а в жидком. В этом случае его доставляют на предприятие в резервуарах и сразу же перекачивают в систему трубопроводов, исключая контакт с персоналом и загрязнение воздуха. [3]
Фталевый ангидрид - один из важнейших видов сырья для производства пластификаторов, лакокрасочных материалов, красителей, лекарственных веществ, инсектицидов, ускорителей вулканизации каучука, присадок к смазочным маслам, добавок к реактивным топливам и др. До недавнего времени фталевый ангидрид получали только из нафталина. [4]
Фталевый ангидрид из о-ксилола можно получать окислением его в паровой или жидкой фазах. В СССР в настоящее время все производство фталевого ангидрида также базируется на парофазном: способе, который не отвечает современным требованиям, так как не позволяет создавать агрегаты большой мощности. Серьезным недостатком парофазного процесса являются также era взрывоопасность и необходимость работы с большим избытком воздуха, что снижает эффективность использования реакционного объема и создает большие трудности при выделении фталевого ангидрида из разбавленной смеси. Проведение процесса окисления в паровой фазе при высокой температуре ( 450 С) приводит к сгоранию значительной части сырья и превращению го в побочные продукты. [5]
Фталевый ангидрид применяется для производства алкидных и полиэфирных смол, пластификаторов, репеллентов. Малеиновый ангидрид используется в производстве полиэфирных смол и присадок к смазочным маслам. [6]
Фталевый ангидрид о - С6Н4 ( СО) 2О получают газофазным окислением о-ксилола или нафталина. Легко растворим в этаноле, умеренно - в других органических растворителях. Применяют в производстве красителей, алкидных смол, пластификаторов, инсектицидов, лекарственных веществ. [7]
Фталевый ангидрид, как известно, находит широкое применение в производстве высококачественных алкидных смол и в настоящее время получается окислением нафталина. [8]
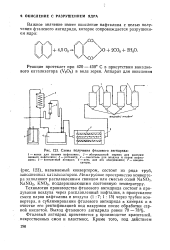 |
Схема получения фталевого ангидрида. [9] |
Фталевый ангидрид применяется в производстве красителей, искусственных смол и пластмасс. [10]
Фталевый ангидрид производят и двухстадийным синтезом - первую стадию окисления проводят в присутствии нафте-ната кобальта при 120 С. При этом образуется о-толуиловая кислота. На второй стадии о-толуиловую кислоту окисляют во фталевый ангидрид при 475 С на пятиокиси ванадия, нанесенной на карборунд. [11]
Фталевый ангидрид легко получают методом окисления в паровой фазе, поскольку он летуч и легко удаляется из слоя катализатора. Изофталевые и терефталевые кислоты значительно менее летучи, они остаются в слое катализатора и подвергаются дальнейшему окислению, поэтому для получения этих соединений применяют процесс окисления в жидкой фазе ( гл. Окисление в жидкой фазе можно применять и для получения фталевого ангидрида, и часть его именно так и получают из смесей ксилолов. Однако, в основном фталевый ангидрид получают окислением в паровой фазе. [12]
Фталевый ангидрид, из которого можно получить фталевую кислоту, легко получается с низкой себестоимостью путем каталитического окисления нафталина воздухом. Сложные эфиры этой кистоты употребляются в качестве пластификаторов. [13]
Фталевый ангидрид в отличие от фталевой кислоты не содержит свободных гидроксильных групп и вследствие этого лучше растворим в неполярных растворителях, например в бензоле. [14]
Фталевый ангидрид легко образуется при нагревании о-фталевой кислоты ( см. опыт 190), он способен вступать в реакции конденсации со многими фенолами ( с незамещенным атомом водорода в пара-положении), образуя производные трифенилметана. Конденсация сопровождается отщеплением воды за счет кислорода одной из карбонильных групп ангидрида и подвижных атомов водорода бензольных ядер двух молекул фенола. Введение водоотнимающих средств, таких, как концентрированная серная кислота или хлористый цинк, значительно облегчает эту конденсацию. [15]
Страницы: 1 2 3 4