Избыток - натрий
Cтраница 3
Кристалл хлорида натрия, нагретый в парах металлического натрия, поглощает последний, так что в кристалле отношение Na / Cl становится больше 1 ( избыток натрия по отношению к сте-хиометрическому составу соответствует 1016 - 1019 дополнительных атомов натрия в 1 см3; это отвечает формуле Nai 0ooooi - i ooiCl); при этом кристалл синеет и становится электронным полупроводником; его плотность уменьшается. [31]
 |
Прибор для получения оксида натрия. [32] |
Нельзя получать чистый Na2O непосредственным окислением металлического натрия, так как при этом одновременно образуется пероксид, который очень трудно восстановить до Na2O путем добавления избытка натрия. [33]
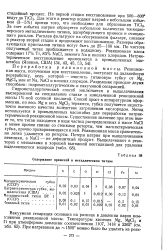 |
Содержание примесей в металлическом титане. [34] |
Для этого в реактор подают натрий с небольшим избытком ( 3 - 5 %) против того, что необходимо для образования TiCl За счет избытка натрия образуется небольшое количество тонкодисперсного металлического титана, адсорбирующего примеси и очищающего расплав. Расплав фильтруют на обогреваемом фильтре, сливают в реактор второй стадии и продолжают восстановление. Размеры образующихся кристаллов титана могут быть до 25 - 100 мм. По чистоте получаемый титан приближается к иодидному. Реакционная масса содержит 17 % Ti, 83 % NaCl, немного Na и низших хлоридов. [35]
Для этого в реактор подают натрий с небольшим избытком ( 3 - 5 %) против того, что необходимо для образования TiQ2, За счет избытка натрия образуется небольшое количество тонкодисперсного металлического титана, адсорбирующего примеси и очищающего расплав. Расплав фильтруют на обогреваемом фильтре, сливают в реактор второй стадии и продолжают восстановление. Размеры образующихся кристаллов титана могут быть до 25 - 100 мм. По чистоте получаемый титан приближается к иодидному. Реакционная масса содержит 17 % Ti, 83 % NaCl, немного Na и низших хлоридов. [36]
Так как фториды остальных щелочных металлов в этих уел виях не осаждаются, данную реакцию можно применять д, отделения их от лития, если только нет избытка натрия. [37]
Как видно из табл. 5, при одинаковых условиях опыта и небольшом избытке натрия ( 1: 1 5) по отношению к тиолам глубина их извлечения растет медленно; при увеличении избытка натрия ( 1: 2) она резко повышается, доходя до определенного максимума, и при дальнейшем увеличении избытка натрия процент связывания тиолов из дистиллята практически не увеличивается. [38]
Как видно из табл. 5, при одинаковых условиях опыта и небольшом избытке натрия ( 1: 1 5) по отношению к тиолам глубина их извлечения растет медленно; при увеличении избытка натрия ( 1: 2) она резко повышается, доходя до определенного максимума, и при дальнейшем увеличении избытка натрия процент связывания тиолов из дистиллята практически не увеличивается. [39]
Далее Кноп ( и другие исследователи) вскоре столкнулся со следующим обстоятельством: помимо исходной реакции, пришлось считаться с той тенденцией к ее изменению, которая зависит от неодинакового восприятия растениями основания и кислоты из отдельных солей; так, если дать растениям азот и в виде NaNOg, то растение будет быстро поглощать азотную кислоту и перерабатывать ее в органические соединения, в растворе же останется избыток натрия, хотя он и будет находиться не в виде свободной щелочи, а будет соединяться с углекислотой, выделяемой корнями, все же раствор будет становиться щелочным; а так как растения обычно требуют азота больше, чем калия и фосфора ( и тем более серы, магния, железа), то от источника азота и зависит больше всего изменение реакции раствора. Поэтому первые исследователи предпочли работать с нитратами, так как тенденция к щелочности смягчается избыточной углекислотой, выделяемой растениями ( образуются бикарбонаты), а кроме того, введение Кнопом в практику водных культур кислого фосфата калия придавало исходному раствору кислую реакцию; поэтому остатки оснований, получающиеся при использовании растением нитратов, вызывают постепенный переход к нейтральной реакции. [40]
Этот метод дает хорошие результаты также и дри восстановлений нитрилов до аминов, причем лучше применять амиловый спирт вместо-этилового 18 или проводить реакцию: в среде ксилола. Избыток натрия при этом должен быть минимальным, вовремя реакции по возможности коротким; после окончания реакции смесь -: нужно. [41]
С и карбонизуют свежеизмельченным сухим льдом. Избыток натрия разрушают 20 мл спирта. [42]
Выделение водорода кончается через 3 - 4 часа. Избыток натрия извлекают оттянутой стеклянной палочкой вплоть до нескольких дециграмм; потом, раствор выпаривают под уменьшенным давление1 до консистенции сиропа, смешивают с И г йодистого метила ( 2 мол. [43]
Ацетиленид натрия получается при добавлении раствора натрия в жидком аммиаке с такой скоростью, чтобы в реакционной смеси не было избытка растворенного натрия. Избыток натрия вызывает появление голубой окраски. [44]
Избыток натрия или калия может быть удален обработкой спиртом. Затем осадок промывают эфиром и высушивают. [45]
Страницы: 1 2 3