Диоксен
Cтраница 1
Диоксен получают путем циклизации и дегидрирования диэтиленгликоля на медном катализаторе в токе водорода в реакторе из термостойкого стекла, изображенном на рисунке. Испаритель и каталитическая зона реактора обогреваются электрическими спиралями, напряжение па которых регулируют с помощью лабораторных автотрансформаторов. В схему прибора входит также источник водорода ( баллон с редуктором), реометр и счетчики пузырьков, которые ставятся на входе и выходе из реактора для контроля поступления водорода в реактор и наблюдения за процессом. Остаточные газы после конденсации диоксена выводятся под тягу. [1]
Диоксен в противоположность 1 4-диоксену еще не был получен. [2]
Диоксен получают путем циклизации и дегидрирования диэтиленгликоля на медном катализаторе в токе водорода в реакторе из термостойкого стекла, изображенном на рисунке. Испаритель и каталитическая зона реактора обогреваются электрическими спиралями, напряжение на которых регулируют с помощью лабораторных автотрансформаторов. В схему прибора входит также источник водорода ( баллон с редуктором), реометр и счетчики пузырьков, которые ставятся на входе и выходе из реактора для контроля поступления водорода в реактор и наблюдения за процессом. Остаточные газы после конденсации диоксена выводятся под тягу. [3]
Диоксен в противоположность 1 4-диоксену еще не был получен. [4]
Реакции этих диоксенов сходны с реакциями кетенов. Они неустойчивы в водных растворах щелочей и кислот и не взаимодействуют с реактивами на карбонильную группу. [5]
Надбензойная кислота окисляет диоксен в глицериновый альдегид. Бром количественно присоединяется к двойной связи. Восстановление в присутствии палладия в спиртовом растворе дает 2-фенил - 1 3-диоксан. [6]
Кроме родоначального соединения-1 4-диоксена - известно большое число замещенных диоксенов. [7]
 |
Диалкил-2 - ациликсиэтилфосфонаты RCOOCH2CH2P ( 0 ( OR 2, полученные присоединением диалкилфосфитов к винилпропионату, -. и йинцлбумфату. [8] |
Диоксаны с фосфонатной группой можно получить также лрисоединением диалкилфосфитов к диоксену. Реакция идет при 90 - 95 С в течение 10 час. [9]
Кислородсодержащие гетероциклы как 1 3 - 1 4-диоксан, дик-садиен, диоксен, пиран [6-12] и 1, 3, 5-триоксан [13, 14] применяются для стабилизации метилхлороформа и перхлорэтилена. [10]
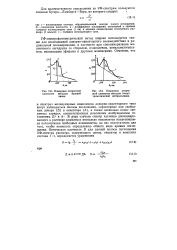 |
Измерение оптической.| Измерение оптической плотности методом гетерохроматической экстраполяции. [11] |
УФ-спектрофотометрический метод широко используется также для исследований донорно-акцепторного взаимодействия в радикальной полимеризации, в частности при сополимеризации ма-леинового ангидрида со стиролом, n - диоксеном, винилциклогекса-ном, виниловыми эфирами и другими мономерами. [12]
Продукты присоединения бесцветны или слабо окрашены в желтый цвет; многие из них при относительно низких температурах распадаются, например, 2 3-дифенилфенантро - ( 9, 10) диоксен ( ХХ1П) уже при 270 распадается на фенантренхинон и стильбен [43], Объяснения термической нестойкости этих производных 1 4-диоксена пока еще нет. [13]
В полулитровую круглодонную трехгорлую колбу, снабженную мешалкой, термометром и обратным холодильником, помещают последовательно 50 мл хлороформа, 150 мл хлористого метилена, 2 0 г хлористого триэтилбензиламмония ( ТЭБА), 43 0 г ( 0 5 моля) диоксена ( см. Синтезы гетероциклических соединений, вып. Органический слой отделяют, дважды промывают водой ( по 150 мл) и сушат над сульфатом магния. После отгонки растворителя остаток перегоняют, собирая фракцию, кипящую при 86 - 88712 мм. [14]
В полулитровую круглодонную трехгорлую колбу, снабженную мешалкой, термометром и обратным холодильником, помещают последовательно 50 мл хлороформа, 150 мл хлористого метилена, 2 0 г хлористого триэтилбензиламмония ( ТЭБА), 43 0 г ( 0 5 моля) диоксена ( см. Синтезы гетероциклических соединений, вып. Органический слой отделяют, дважды промывают водой ( по 150-мл) и сушат над сульфатом магния. После отгонки растворителя остаток перегоняют, собирая фракцию, кипящую при 86 - 88 / 12 мм. [15]
Страницы: 1 2