Извлечение - таллий
Cтраница 3
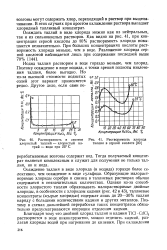 |
Растворимость в системе хлористый таллий - хлористый натрий - вода при 25 С. [31] |
Иодид таллия растворим в воде гораздо меньше, чем хлорид. Поэтому осаждение в виде иодида, с точки зрения полноты извлечения таллия, более выгодно. Но из-за высокой стоимости йодистых солей этот вариант применяется редко. [32]
Степень разбавления была выбрана в соответствии с данными о зависимости степени извлечения таллия ( III) и примесей в органическую фазу от концентрации ТБФ. [33]
Во многих случаях реализуется только часть кривой экстракции. Если одновременно экстрагируются координационно сольватированные соединения и комплексные кислоты, то чаще всего получаются кривые типа 1 или 2 как, например, при извлечении таллия ( III) из галогенидных растворов ТБФ. [34]
Трилоновые комплексы этих элементов не экстрагируются расплавами дифениламина и полностью остаются в водном слое. В этих условиях при отношениях Т13: РЬ2 1: 200; TI3: Zn2, Cd2 1: 200, Т13: Cu2, Fe3 1: 300 извлечение таллия органическим слоем достигает 99 % при однократной экстракции. [35]
Таллий легко переходит обратно в раствор в результате окисления. Если в растворе, откуда цементируют таллий, есть металлы с низким перенапряжением водорода ( такие, как медь и никель), возможно обратное растворение губки с выделением водорода. Для извлечения таллия кадмиево-таллиевую губку растворяют в серной кислоте; из раствора, добавляя Nal или К2Сг2О7, осаждают таллиевый концентрат, который затем перерабатывают по уже описанным схемам. [36]
Например, для извлечения таллия из агломерационных пылей свинцового производства предложена следующая схема. Растворы, полученные в результате водного выщелачивания пылей, подкисляются серной кислотой до 5 г / л и подвергаются взаимодействию с цинковой амальгамой при энергичном перемешивании. [37]
Окислительно-восстановительные реакции металлов с окислами таллия и марганца сильно облегчают растворение тех и других продуктов. Выделяющийся при растворении металлов водород является дополнительным восстановителем. Дальнейшая переработка полученных растворов с целью извлечения таллия производится уже известными методами. [38]
Хотя таллий и образует несколько минералов, например лоран-дит TlAsS2 и крукезит ( Tl Cu, Ag) 2Se, они также весьма редки. Это подтверждается валовым составом указанных минералов. Основным сырьем для получения таллия служат полиметаллические руды, в которых он присутствует в виде примеси. Извлечение таллия из пыли, получающейся при окислительном обжиге этих руд, основано на растворимости оксида таллия в горячей воде. Полученный гидроксид переводят в сульфат таллия, который и подвергают электролизу. Существуют способы, по которым сначала получают плохо растворимый Т1С1, который восстанавливают до металла цинком. Возможно также восстановление оксида таллия углем или водородом. [39]
Хотя таллий и образует несколько минералов, например лорандит TlAsS2 и крукезит ( Tl Cu Ag) 2Se, они также весьма редки. Это подтверждается валовым составом указанных минералов. Основным сырьем для получения таллия служат полиметаллические руды, в которых он присутствует в виде примеси. Извлечение таллия из пыли, получающейся при окислительном обжиге этих руд, основано на растворимости оксида таллия в горячей воде. Полученный гидрок-сид переводят в сульфат таллия, который и подвергают электролизу. [40]
Хотя таллий и образует несколько минералов, например лорандит TIAsSa и крукезит ( Tl Cu Ag) 2Se, они также весьма редки. Это подтверждается валовым составом указанных минералов. Основным сырьем для получения таллия служат полиметаллические руды, в которых он присутствует в виде примеси. Извлечение таллия из пыли, получающейся при окислительном обжиге этих руд. Полученный гидрок-сид переводят в сульфат таллия, который и подвергают электролизу. [41]
Ионнообменные методы нашли широкое применение в процессах извлечения таллия из полупродуктов, из технологических сточных вод, а также при получении наиболее важных химических соединений элемента. Исследователи установили, что в силу высокого ионообменного сродства ионов Т1 целый ряд катио-нитов очень сильно проявляет свои селективные свойства к таллию. Особенно высоким избирательным действием по отношению к одновалентному таллию обладают катиониты, содержащие группы - ОН и - СООН. К числу их относится распространенный и дешевый катионит КУ-1 - Избирательность катионитов дает возможность применять их для извлечения таллия из производственных растворов сложного химического состава. [42]
Таллий выщелачивается значительно легче индия. Только и само выщелачивание, и отделение раствора от остатка нужно проводить при нагревании, так как растворимость хлорида таллия сильно зависит от температуры. Иногда вместо водного выщелачивания применяют выщелачивание слабыми содовыми растворами. При этом несколько увеличивается извлечение таллия в раствор, по-видимому, за счет разложения малорастворимого арсенита таллия. Если таллий присутствует в виде труднорастворимых соединений, то применяют выщелачивание разбавленной серной кислотой. Более полного извлечения можно достичь сульфатизацией пылей в кипящем слое после грануляции с крепкой серной кислотой, как это описано в разделе, посвященном индию. [43]
Страницы: 1 2 3