Диоксид - германий
Cтраница 3
Для создания собственного защитного покрытия на германии используют фазовое превращение гексагонального диоксида германия в более плотную и стабильную тетрагональную модификацию в процессе длительного отжига при температуре 700 - 750 С. [31]
Окисление германия происходит последовательно - вначале до монооксида, а затем до диоксида германия. Диоксид германия неустойчив в водной среде и легко связывается в устойчивый водорастворимый комплекс H2GeO3 ( метагерма-ниевая кислота), который может частично диссоциировать. Видно, что окисление, комплексообразование и восстановление окислителя происходит одновременно в ходе поверхностной окислительно-восстановительной реакции. Все стадии процесса и процесс в целом подчиняются чисто химическим закономерностям. [32]
 |
Зависимость удельной проводимости полупроводника от напряженности электрического поля при различной температуре окружающей среды ( 7 i Г2.| Схема устройства для зонной плавки. [33] |
В результате химической переработки исходного сырья образуется тетрахлорид германия, который путем дальнейших операций переводят в диоксид германия ( Ge02) - порошок белого цвета. Диоксид германия восстанавливается в водородной печи при температуре 650 - 700 С до элементарного германия, представляющего собой серый порошок. В некоторых случаях порошок германия получают непосредственно из GeQ4 путем разложения этого соединения при высокой температуре в атмосфере паров цинка. Порошок германия подвергают травлению в смеси кислот и сплавляют в слитки. [34]
 |
Зависимость удельной проводимости полупроводника.| Схема устройства для зонной плавки. [35] |
В результате химической переработки исходного сырья образуется тетрахлорид германия, который путем дальнейших операций переводят в диоксид германия ( GeO2) - порошок белого цвета. Диоксид германия восстанавливается в водородной печп при температуре 650 - 700 СС до элементарного германия, представляющего собой серый порошок. В некоторых случаях порошок германия получают непосредственно из GeQ4 путем разложения этого соединения при высокой температуре в атмосфере паров цинка. Порошок германия подвергают травлению в смеси кислот и сплавляют в слитки. [36]
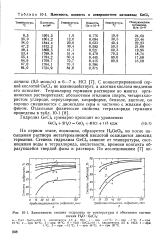 |
Плотность, вязкость и поверхностное натяжение ОеСЦ.| Зависимость степени гидролиза от температуры и объемного соотношения Н. гО. ОеСЦ. [37] |
На первом этапе, возможно, образуется H2GeO3, но после насыщения раствора метагерманиевой, кислотой осаждается диоксид германия. Степень гидролиза GeCU зависит от температуры, соотношения воды и тетрахлорида, кислотности, времени контакта образующейся твердой фазы и раствора. [38]
Тетрахлорид германия получают главным образом из герма-нийсодержащих концентратов и шлаков, а в отдельных случаях из металлического германия, моно - и диоксида германия. [39]
Окисление германия происходит последовательно - вначале до монооксида, а затем до диоксида германия. Диоксид германия неустойчив в водной среде и легко связывается в устойчивый водорастворимый комплекс H2GeO3 ( метагерма-ниевая кислота), который может частично диссоциировать. Видно, что окисление, комплексообразование и восстановление окислителя происходит одновременно в ходе поверхностной окислительно-восстановительной реакции. Все стадии процесса и процесс в целом подчиняются чисто химическим закономерностям. [40]
В результате химической переработки исходного сырья образуется тетрахлорид германия, который путем дальнейших операций переводят в диоксид германия ( Ge02) - порошок белого цвета. Диоксид германия восстанавливается в водородной печи при температуре 650 - 700 С до элементарного германия, представляющего собой серый порошок. В некоторых случаях порошок германия получают непосредственно из GeQ4 путем разложения этого соединения при высокой температуре в атмосфере паров цинка. Порошок германия подвергают травлению в смеси кислот и сплавляют в слитки. [41]
В результате химической переработки исходного сырья образуется тетрахлорид германия, который путем дальнейших операций переводят в диоксид германия ( GeO2) - порошок белого цвета. Диоксид германия восстанавливается в водородной печп при температуре 650 - 700 СС до элементарного германия, представляющего собой серый порошок. В некоторых случаях порошок германия получают непосредственно из GeQ4 путем разложения этого соединения при высокой температуре в атмосфере паров цинка. Порошок германия подвергают травлению в смеси кислот и сплавляют в слитки. [42]
Германиевые линзы, легированные золотом, являются неотъемлемой частью приборов инфракрасной техники. Из диоксида германия изготовляют специальные оптические стекла с большим коэффициентом преломления. Германий вводят также в состав сплавов для высокочувствительных термопар. [43]
Значительные трудности представляет сохранение германия при озолении, так как многие его соединения обладают высокой летучестью. Менее летуч диоксид германия ( Гпл. Поэтому для предотвращения потерь германия пробу обрабатывают окислительной смесью. Твердый или высоковязкий продукт осторожно нагревают до размягчения. Смесь сверху засыпают тонким слоем оксида магния и выдерживают 6 - 7 суток при температуре не выше 200 С. При этом следят, чтобы из смеси не выделялся дым. Затем чашку переносят в холодную муфельную печь и, медленно поднимая температуру, доокиеляют пробу до ее полного обесцвечивания. Установлено, что при прямом озолении пробы содержащийся в ней германий практически полностью теряется. Когда выпаривают пробу нефти до мазута и сжигают мазут с окислительной смесью, теряется до 50 % германия. [44]
Черно-коричневый РЬО2 при нагревании разлагается. Подобно SiO2 диоксид германия легко переходит в стеклообразное состояние. При добавке диоксида германия в кварцевое стекло получаются очень прозрачные, сильно преломляющие свет стекла, что определяет важное значение Ge02 в производстве оптического стекла. [45]
Страницы: 1 2 3 4