Излом - кондуктометрическая кривая
Cтраница 2
Построение кривых титрования показало, что кондуктометры-ческое титрование позволяет проводить анализ смесей слабых кислот с рКа Ю, имеющих ЛрКа: 2 и отличающихся подвижно-стями анионов. Вместе с тем следует отметить, что углы излома кондуктометрических кривых в первой точке эквивалентности очень тупые, так как подвижности анионов в водных растворах, в общем, мало различаются, что затрудняет применение кондуктомет-рического метода для анализа смесей слабых кислот в водных растворах. [16]
Продолжительность титрования определяют по хронокондукто-метрическим кривым, которые в большинстве случаев автоматически наносятся на диаграммную ленту самопишущего прибора. При точечной записи кривой находят число интервалов от начала титрования до излома кондуктометрической кривой. Умножив эту величину на время между записью показаний, определяют продолжительность титрования. Если ведут непрерывную запись кривой титрования, находят длину диаграммной ленты, соответствующую титрованию определяемого вещества. [17]
Например, ДрКа уксусной ( рКа 4 75) и борной ( р / С0 9 12) кислот составляет достаточно большую величину. Однако при титровании смеси этих кислот ( рис. 19 6) окончание нейтрализации уксусной кислоты не фиксируется четким изломом кондуктометрической кривой, потому что мало отличаются подвижности анионов титруемых кислот. [18]
В тех случаях, когда электролиты характеризуются значением ( рКа рКь) 16, в первой точке эквивалентности в растворе находится смесь слабой кислоты и слабого основания. Некоторое количество катионов слабого основания и анионов слабой кислоты, которое имеется в растворе, вызывает слабое закругление излома кондуктометрической кривой около первой точки эквивалентности. [19]
Кривая титрования до первой точки эквивалентности имеет слабый изгиб, что объясняется уменьшением силы НС1 в ацетоно-водной среде. Затем последовательно нейтрализуются СН3СООН и Н3ВО3; повышение электропроводности раствора при нейтрализации СН3СООН сильнее выражено, что приводит к появлению второго излома кондуктометрической кривой. При избытке щелочи наблюдается резкое повышение электропроводности раствора. На кондуктометрических кривых графическим методом устанавливают точки эквивалентности и определяют число интервалов между изломами. Отсчет начинают со второй точки. Десятые доли интервалов вблизи точек эквивалентности определяют на глаз. При этом в расчетную формулу вводят число интервалов, соответствующих титрованию отдельных кислот, их грамм-эквиваленты и нормальность NaOH, как указано выше, по метиловому оранжевому или фенолфталеину. [20]
Так, в смесях с сильными одноосновными и двухосновными кислотами определяются: янтарная ( рКа - 4 21; 5 64), глутаровая ( рКа 4 34; 5 22), адипиновая ( рКа - 4 42; 5 28) и многие другие. Титрование слабых двухосновных кислот по ступеням нейтрализации даже при достаточной разнице в их константах диссоциации в большинстве случаев не приводит к заметным изломам кондуктометрической кривой, так как, в общем, подвижности НАгг - и Ап - - - ионов, образующихся в процессе реакции, недостаточно сильно различаются. [21]
Двухосновные кислоты, достаточно хорошо диссоциирующие по первой ступени ( р / Сд 2 5), но слабо диссоциирующие по второй ступени ( рК а. Если кислота сильно диссоциирована по первой ступени и слабо по второй, наблюдается линейное понижение электропроводности до первого излома и линейное повышение электропроводности до второго излома кондуктометрической кривой. Уменьшение степени диссоциации кислоты по первой ступени приводит к изгибу кондуктометрической кривой до первой точки эквивалентности. [22]
При хронокондуктометрическом титровании в расчетах используют другие зависимости. Расчеты основываются на времени титрования. Если осуществляют непрерывную запись кондуктометрических кривых, время титрования пропорционально длине диаграммной ленты от начала титрования до излома кондуктометрической кривой. [23]
Соли, образованные кислотами, сравнительно хорошо диссоциирую щими по первой ступени ( р / Са2 5) и слабо - по второй ( pJ c 4), количественно взаимодействуют с титрантом, образуя кислые соли. Если кислоты по первой ступени сильно диссоциированы, при взаимодействии их солей с сильной кислотой образуются только НАгг-ионы и после точки эквивалентности электропроводность линейно увеличивается от избытка титранта. Если же диссоциация двухосновной кислоты по первой ступени неполная ( значение р / Сд приближается к 2 5), после излома кондуктометрической кривой в точке эквивалентности, соответствующей образованию кислой1 соли, электропроводность изменяется нелинейно, появляется небольшой изгиб кривой вследствие образования некоторого количества молекул слабой кислоты. Однако при АрКа - 2 в этом случае возможно установить точку эквивалентности, соответствующую кислой соли. [24]
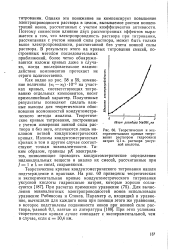 |
Теоретическая и экспериментальная кривые титрования раствором гидроокиси натрия 0 1 н. раствора уксусной кислоты. [25] |
Как видно из рис. 58 и 59, изменение величины ( KI - 3 2) - Ю 3 на участках кривых, соответствующих титрованию отдельных компонентов, носит прямолинейный характер. Полученные результаты позволяют сделать важные выводы для теоретичгского обоснования возможностей кондуктометри-ческого метода анализа. Теоретические кривые титрования, построенные с учетом измерения ионной силы раствора и без него, отличаются лишь наклоном ветвей кондуктометрических кривых. Изломы кондуктометрических кривых в том и другом случае соответствуют точкам эквивалентности. Таким образом, границы р / С электролитов, позволяющие проводить кондуктометрические определения индивидуальных веществ и анализ их смесей, рассчитанные при / 1 и А, const, сохраняются. [26]
Кривая титрования щелочью смеси НС1 и аминоуксус-иой кислоты ( 2: 1) ( р / ( а / 2 35 и p / V 4 22) ( рис. 19, кривая 2) типична для смесей цвиттерионов с сильными кислотами. Сначала наблюдается резкое понижение электропроводности раствора, что связано с нейтрализацией имеющихся в растворе ионов водорода. Кондукто-метрическая кривая до первого излома изогнута, что объясняется уменьшением степени диссоциации карбоксильных групп с увеличением в растворе концентрации цвиттерионов. После излома кондуктометрической кривой протекает реакция вытеснения аминогрупп, что сопровождается повышением электропроводности раствора, так как при этом цвиттерионы переходят в анионы. [27]
До точки эквивалентности концентрация ацетат-ионов падает, а ионов натрия - растет, что компенсирует влияние каждого из них на электропроводность раствора. Поэтому до точки эквивалентности электропроводность раствора мало изменяется. Пзлом кондуктометрической кривой в точке эквивалентности можно объяснить ростом концентрации ацетат-ионов и ионов натрия после точки эквивалентности, что приводит к повышению электропроводности раствора. Так как раствор с начала титрования имеет высокую электропроводность, угол излома кондуктометрической кривой тупой. [28]
В ячейку для титрования наливают 25 мл раствора гидрохлорида диэтиламина и 25 мл ацетона, погружают электроды и мешалку, включают мотор для вращения ячейки и милливольтметр. Раствор перемешивают несколько минут для достижения постоянной электропроводности и при помощи делителя напряжений стрелку милливольтметра устанавливают в верхней части шкалы. Включают регистрирующую часть милливольтметра и при нанесении второго показания на ленту начинают подачу раствора NaOH. После окончания титрования поднимают кронштейн с электродами и вынимают их из ячейки. Электроды, мешалку и ячейку тщательно промывают дистиллированной водой и проводят параллельное определение. На кондукто-метрических кривых графическим методом устанавливают точки эквивалентности, определяют количество интервалов между точками до излома кондуктометрической кривой и берут среднее значение. Отсчет начинают со второй точки, десятые доли интервала вблизи точки эквивалентности определяют на глаз. Электропроводность сначала пони жается, а после точки эквивалентности быстро возрастает. Кондуктометрическая кривая титрования диэтиламингидрохлорида характеризуется одним изломом. [29]
В ячейку для титрования наливают 25 мл раствора гидрохлорида диэтиламина и 25 мл ацетона, погружают электроды и мешалку, включают мотор для вращения ячейки и милливольтметр. Раствор перемешивают несколько минут для достижения постоянной электропроводности и при помощи делителя напряжений стрелку милливольтметра устанавливают в верхней части шкалы. Включают регистрирующую часть милливольтметра и при нанесении второго показания на ленту начинают подачу раствора NaOH. После окончания титрования поднимают кронштейн с электродами и вынимают их из ячейки. Электроды, мешалку и ячейку тщательно промывают дистиллированной водой и проводят параллельное определение. На кондукто-метрических кривых графическим методом устанавливают точки эквивалентности, определяют число интервалов между точками до излома кондуктометрической кривой и берут среднее значение. Отсчет начинают со второй точки, десятые доли интервала вблизи точки эквивалентности определяют на глаз. Электропроводность сначала понижается, а после точки эквивалентности быстро возрастает. Кондукто-метрическая кривая титрования диэтиламингидрохлорида характеризуется одним изломом. [30]
Страницы: 1 2 3