Сравнение - изотерма - адсорбция
Cтраница 2
Существенная разница поведения углей СКТ-6А и АР-3 объясняется, по-видимому, различиями пористой структуры. Сравнение изотерм адсорбции показывает, что мочевина является наиболее трудно удаляемым метаболитом. При исследовании динамики сорбции и выборе скорости движения жидкой фазы основное внимание поэтому должно быть уделено мочевине. [16]
 |
Кривые поглощения кислорода белым фосфором, нанесенным на пемзу, при различных температурах. / - 60 С. 2 - 24 С. 3 - - - - - - 20 С. [17] |
Для определения кислорода в водороде или гелии кислород предварительно адсорбируют углем при температуре жидкого азота. Сравнение изотерм адсорбции кислорода с изотермами адсорбции водорода и гелия при температуре - 183 С показывает, что при малых давлениях кислород сорбируется в 1000 раз больше, чем водород, и в миллион раз больше, чем гелий. Подготовленную пробу АГС пропускают через раскаленную вольфрамовую спираль. Кислород соединяется с вольфрамом, по изменению давления судят о концентрации кислорода. [18]
Представление о вкладе катионов в энергию адсорбции могут дать измерения адсорбции и теплот адсорбции на изоструктурных цеолитах, различающихся числом одноименных катионов в их элементарных ячейках. Проведенное нами сравнение изотерм адсорбции С02 и NH3 на синтетических фожазитах с различными соотношением Si / Al в их решетках, а поэтому и с различным содержанием обменных катионов в элементарных ячейках, показывает ( рис. 1), что в обоих случаях с ростом катионной плотности наблюдается значительное увеличение адсорбции. [19]
Дубинин считает, что сравнение изотермы адсорбции на адсорбенте с неизвестной величиной поверхности со стандартной изотермой для непористого адсорбента одинаковой химической природы с известной удельной поверхностью - прием вполне законный ( стр. Вместе с тем Русанов ( см. стр. А численное значение этого члена позволило бы судить о степени надежности i-метода де Бура. [20]
Нами предложен метод, основанный на широком использовании приема сравнения. Суть метода заключается в сравнении изотермы адсорбции на образце-эталоне ( анатазе или любом хорошо изученном и сравненном с анатазом адсорбенте) с изотермой адсорбции на исследуемом образце. Если эти изотермы аффинны во всем изученном интервале давлений, то это означает подобие адсорбционных свойств и, значит, соответствующее равенство ют для эталона и образца. [21]
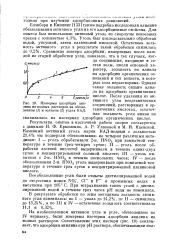 |
Изотермы адсорбции анилина из водных растворов на обезволенном ( 1 и зольном ( 2 углях КАД. [22] |
Блэкберн и Киплинг [133] также подробно исследовали влияние обеззоливания активного угля на его адсорбционные свойства. Уголь был последовательно обработан водой, уксусной, затем плавиковой кислотой. Сравнение изотерм адсорбции, измеренных после каждой из стадий обработки угля, показало, что в тех случаях, когда соединения, входящие в состав золы, имели основной характер, зольность не влияла на адсорбцию органических оснований и тех веществ, в которых зола нерастворима. [23]
Количество адсорбированных паров воды при низких относительных давлениях чрезвычайно мало, в то время как изотермы органических соединений по сравнению с исходным цеолитом NaY указывают лишь на немного меньшую адсорбционную емкость и имеют типичный для цеолитов ход. Сравнение изотерм адсорбции азота на исходном цеолите NaY и на образце 9 деалюминированного цеолита показывает, что в этом образце возникла вторичная пористая структура, вероятно, вследствие кислотной экстракции решеточного алюминия. Сравнение адсорбционной емкости исходного цеолита NaY и образца 8 показывает, что при деалюминировании резко возросла гидрофобность: в то время как для органических паров емкость уменьшилась лишь на 9 - 17 %, для паров воды она уменьшилась в пять раз. При постоянных Т тир десорбция воды с образца 8 происходит значительно легче, чем с NaY. Это различие для воды значительно более существенно, чем для органических паров. [24]
По адсорбционным свойствам ВК-цеолиты мало отличаются друг от друга. В качестве примера на рис. 2 приведены изотермы адсорбции воды, бензола и гексана при 20 С на одном из цеолитов серии ЦВК. Сравнение изотерм адсорбции указанных веществ свидетельствует о гидрофобном характере ВК-цеолитов: вода адсорбируется в значительно меньшем количестве, чем бензол или гексан. При увеличении отношения Si02 / Al203 в цеолите количество адсорбированной воды уменьшается, тогда как адсорбция бензола и гексана не изменяется. Между величиной адсорбции бензола и гексана обнаружено постоянное соотношение: во всех изученных ВК-цеолитах бензол заполняет 60 5 % объема, заполняемого гексаном. [25]
С делает изотерму адсорбции воды близкой к линейной в довольно широком интервале давления пара. Все это указывает на слабую специфичность хромосорба-102. Однако эта специфичность четко выявляется при сравнении изотерм адсорбции диэтилового эфира и н-бутанола, имеющих одинаковые молекулярные веса. [26]
Как видно из рис. 5, повышение а с концентрацией в случае CsF для двух границ раздела различно. ТНЗ смещается в катодную сторону. Как показывает сравнение гиббсовских изотерм адсорбции анионов F - в растворах CsF и KF в зависимости от заряда и концентрации, специфическая адсорбция Cs проявляется не только при е0, но и при любых других зарядах. Во всех случаях специфическая адсорбция Cs ведет к уменьшению отрицательной адсорбции р - - иона. Этот эффект растет с увеличением концентрации и при переходе от положительных к отрицательным зарядам поверхности. [27]
Метод определения инкрементов уменьшения молярной стандартной энергии Гиббса при адсорбции из раствора сводится к сравнению изотерм адсорбции двух, веществ, структура молекул которых отличается только одной деталью структуры, функциональной группой или заместителем. Значения б ( - AG) элемента структуры молекулы, найденные сравнением изотерм адсорбции различных пар веществ из раствора, близки между собой, что является подтверждением достаточно строгого соблюдения аддитивности величины - - AG9. [28]
Метод определения инкрементов уменьшения молярной стандартной энергии Гиббса при адсорбции из раствора сводится к сравнению изотерм адсорбции двух веществ, структура молекул которых отличается только одной деталью структуры, функциональной группой или заместителем. ДО дает значение инкремента уменьшения молярной стандартной энергии Гиббса, обусловленного введением в структуру молекулы этого элемента структуры. Значения б ( - ДО) элемента структуры молекулы, найденные сравнением изотерм адсорбции различных пар веществ из раствора, близки между собой, что является подтверждением достаточно строгого соблюдения аддитивности величины - ДО0. [29]
Страницы: 1 2