Сравнение - константа - скорость - реакция
Cтраница 1
Сравнение констант скоростей реакции хлористого бензила с пиридином ( 22.8 - Ю 5 л / моль-мин. [1]
Сравнение констант скоростей реакций I, II и III показывает, что наиболее благоприятное равновесие устанавливается в случае гидрокарбометоксилирования, наименее - при гидроформили-ровании бутадиена. Это явление аналогично наблюдаемому [2, 3] при подобных реакциях этилена. [2]
Из сравнения констант скоростей реакции окисления видно, что волновое воздействие ускоряет процесс окисления нефтяного остатка почти в два раза. [3]
Такие сравнения констант скоростей реакции различных мономеров с ОН-ра-дикалами позволяют использовать полярографический метод для характеристики реакционной способности мономеров. [4]
При сравнений констант скоростей реакции окисления при акустическом воздействии и механическом перемешивании видно, что скорость реакции при акустическом воздействии на три порядка выше чем механическом перемешивании. [5]
Так, сравнение констант скоростей реакций с участием этилендиамина и этиламина показывает, что наличие одного азотного атома в р-положении приблизительно в 2 раза снижает скорость превращения. Очевидно, что для нуклеофилов VII и VIII соответствующее снижение константы скорости должно быть четырех - и восьмикратным. [6]
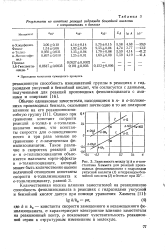 |
Зависимость между lg k и сг-кон-стантами Хаммета для реакций производных фенилизоцианата с гидразидом уксусной кислоты ( / и гидразидом бензойной кислоты ( 2 в бензоле при 25. [7] |
Однако при сравнении констант скорости реакций n - толил - и о-толилизо-цианатов видно, что константы скорости для о-замещенного почти в три раза меньше по сравнению с n - замещенным фе-нилизоцианатом. [8]
 |
Энтропии полимеризации и адсорбции В А и ММА на поверхности и в жидкой фазе ( значение энтропии мономеров в газовой фазе условно принято за 0. М и П - мономер и полимер. [9] |
Таким образом, проведенные расчеты показывают, что сравнение констант скорости реакции роста на поверхности и в объеме следует проводить с учетом конкретного механизма адсорбции данного мономера. [10]
Для нас представляют прямой интерес результаты обширных работ но сравнению констант скоростей реакций кислотно-основного катализа с протием, дейтерием и тритием. [11]
Это позволяет определить константы скорости при нулевой ионной силе, что необходимо для сравнения констант скоростей реакций в неводных растворителях, получаемых в различных условиях. [12]
Рассмотренные данные свидетельствуют о том, что при изучении зависимости между строением фосфорсодержащих соединений и реакционной способностью те представления об электронном влиянии заместителей, которые основаны на сравнении констант скоростей реакций, определенных только при одной температуре, являются недостаточно полными, энергия и энтропия активации более чувствительны к влиянию заместителей на перераспределение электронов в переходном состоянии нуклеофильного замещения у тетраэдрического атома фосфора. [13]
Это лишний раз подтверждает ранее высказанное предположение о том, что представления об электронном влиянии заместителей, связанных с фосфором, на реакционную способность фосфорсодержащих соединений, основанные на сравнении констант скоростей реакции только при одной температуре, будут недостаточно полными. [14]
Показано, что реакции гидролиза подчиняются уравнению реакции первого порядка. Результаты сравнения констант скоростей реакций отщепления формальдегида в этих средах согласуются с данными о химической стойкости ацетальных связей. [15]
Страницы: 1 2