Сравнение - молекула
Cтраница 1
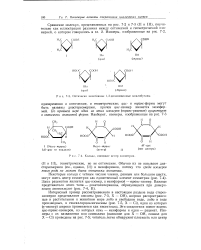 |
Кольца, имеющие центр симметрии. [1] |
Сравнение молекул, представленных на рис. 7 - 2 и 7 - 3 ( II и III), поучительно как иллюстрация различия между оптической и геометрической изомерией, о котором говорилось в гл. [2]
При сравнении молекул дигидрофолат-редуктазы из различных источников сразу же обращает на себя внимание очень близкое сходство их общей формы и укладки пептидных цепей. Ясно, что за миллионы лет эволюции структура фермента почти не претерпела изменений, несмотря даже на то, что неизменными во всех ферментах сохраняются только 25 % аминокислотных последовательностей. [3]
При сравнении молекул СО и СО2 [210] бросается в глаза тот факт, что длина связи СО приблизительно одна и та же в обеих молекулах. Кроме того, ультрафиолетовый спектр поглощения свидетельствует о том, что результирующий заряд на атоме кислорода в обоих случаях практически один и тот же ( см. стр. Это означает, что плотность зарядового облака между атомами О и С и вблизи ядра атома О должна быть практически одинаковой в обеих молекулах. Конечно, плотности могут быть различными вблизи ядра атома С. [4]
При сравнении молекул дигидрофолат-редуктазы из различных источников сразу же обращает на себя внимание очень близкое сходство их общей формы и укладки пептидных цепей. Ясно, что за миллионы лет эволюции структура фермента почти не претерпела изменений, несмотря даже на то, что неизменными во всех ферментах сохраняются только 25 % аминокислотных последовательностей. [5]
 |
Схема строения молекулы этилена ( мономер и молекулы полиэтилена ( полимер. [6] |
На рис. 70 схематически показано сравнение молекулы газа этилена и молекулы твердого и пластичного полиэтилена. Молекулы полиэтилена образуются в результате химической реакции, при которой под влиянием нагрева, давления и действия катализатора молекулы этилена последовательно соединяются без образования побочных продуктов. [7]
 |
Сравнение аюмеров Сахаров. [8] |
Так как прямым экспериментальным путем невозможно найти величины молярных долей вращения оптических центров, то правильность принципа Вант-Гоффа была показана на примере сравнения молекулы. А В С центров, с молекулой, [ M ] D которой слагается из молекулярных долей ротофоров - A iB C. [9]
Так как прямым экспериментальным путем невозможно найти величины молярных долей вращения оптических центров, то правильность принципа Вант-Гоффа была показана на ( примере сравнения молекулы, [ M ] D которой слагается из А В С центров, с молекулой [ Що которой слагается из молекулярных долей ротофоров - А В С. [10]
При отсутствии точных данных, позволяющих перейти от Кл к / Ci и / С2, величины / Cd представляют интерес в основном для сравнения родственных молекул, для которых на основании сходства их геометрии и общего подобия возможно считать, что / С2 имеет постоянную величину. [11]
Вандерваальсовы силы и размер молекул. Путем сравнения сходных молекул установлено, что большая молекула будет иметь более высокую температуру плавления. Это различие объясняется тем, что у двух молекул этана большая поверхность контакта, чем у двух молекул метана. [12]
ИК-спектрам) может быть проведена только при сопоставлении с подлинным эталонным спектром. Эти спектры служат и другой полезной цели, даже если точное соответствие не найдено; они указывают путь к вероятным структурам ( или помогают исключить постулированные структуры) путем сравнения сходных молекул, содержащих некоторые одинаковые группы. Для опытного спектроскописта библиотека эталонных спектров так же важна, как и спектрофотометр. [13]
Распространив теорию химического строения на область непредельных ( этиленовых и ацетиленовых) соединений, Бутлеров показал зависимость явлений полимеризации от неустойчивости и непредельности органических соединений. Придавая большое значение изучению вопроса о том, почему одни молекулы устойчивы, а другие нет, Бутлеров в 1864 г. писал: Почему одни молекулы не способны, а другие способны к существованию. Разрешению последнего вопроса должно помочь сравнение теоретически возможных молекул с действительно существующими, связанное с тщательным исследованием других химических и физических отношений тел in statu quo и во время химических процессов, и это, на мой взгляд, один из наиболее важных шагов, которые наука в ближайшем будущем должна сделать [ 7, стр. [14]
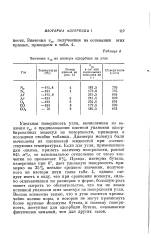 |
Значения г ив изотерм адсорбции на угле. [15] |
Страницы: 1 2