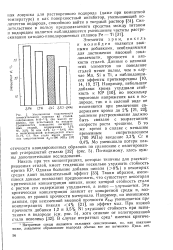
Нитратная среда
Cтраница 1
Нитратные среды являются сильными окислителями, но, как показано ниже, локальное образование водорода обычно все же возможно. [2]
 |
Объемные коэффициенты распределения в растворе HCl - fHF. концентрация НС1 от 0 1 до 12 М. [3] |
Нитратная среда при анионном обмене имеет меньшее значение, чем хлоридная и смешанная хлоридно-фторидная, так как лишь несколько элементов образуют устойчивые нитратные комплексы. [4]
Кроме нитратных сред в последнее время изучается экстракция из перхлоратного [1810] и хлоридного [1169, 1843] растворов, причем в некоторых случаях появляются возможности, например, для отделения Sc [1580] и Fe [1101] от Y. Во второй методике используется родственный трибутилфосфату нейтральный экстрагент три-н. [5]
Из нитратных сред экстрагируются координационно-сольва-ткрованные сульфоксидами соли, поэтому экстракция большинства металлов из нитратных среде небольшой и постоянной ионной силой не зависит от варьирования концентрации водородных ионов. При экстракции циркония, гафния с ростом концентрации водородных ионов происходит увеличение коэффициента распределения ( Д), что связано, по-видимому, с плохой экстракцией присутствующих гидролизованных форм катионов данных металлов при низких концентрациях водородных ионов. При извлечении из хлоридных растворов сульфоксиды, по аналогии с ТБФ, могут экстрагировать хлориды металлов по двум механизмам: в виде координациошю-сольватирорзнных соединений МеХ qS и комплексных анионов, входящих в состав ионных ассопиатов. [6]
В нитратной среде выполняются и некоторые другие разделения. К их числу относится отделение железа от следовых количеств свинца, марганца, меди, никеля, цинка и титана. Однако эти разделения не типичны для элементов, рассматриваемых в настоящем разделе; гораздо чаще используются такие среды, в которых эти элементы образуют прочные комплексы. [7]
Количественное осаждение трехвалентного плутония из нитратных сред имеет то преимущество, что плутоний весьма просто переводится в трехвалентное состояние. Чаще всего в практике используют именно осаждение сульфатов трехвалентного плутония. [8]
Удобным методом концентрирования является экстракция ТБФ из нитратной среды, которая упоминалась выше. При работе с роданидом следует избегать больших концентраций кислоты и сильных окислителей. [9]
Кроме названных работ по отделению урана в нитратных средах, следует упомянуть метод Новака и Пекарека [169] отделения урана от ряда элементов на анионите в хлоридно-нитратных смесях. [10]
Методы экстракции плутония и других четырех - и шестивалентных актинидов из нитратных сред довольно селективны, так как многие двух - и трехвалентные элементы в этих условиях не экстрагируются. [11]
Было выяснено, что гидролизованные катионы металлов лучше всего извлекаются из нитратных сред, плохо из сульфатных. Из нитратных сред хорошо извлекаются висмут ( III), железо ( III), медь, кобальт, цинк, никель, хуже цирконий и гафний. Состав экстрагируемых комплексов был установлен, как непосредственным химическим анализом, так и методом сдвига равновесия. [12]
Майорова и Фомин [341] по изменению коэффициента распределения тория при экстракции из нитратных сред трибутил-фосфатом в присутствии сульфат-иона нашли состав и константы устойчивости смешанных нитратосульфатных комплексов тория. [13]
В работе [133] были получены данные о скорости экстракции U, Pu, Ru и Zr из нитратных сред растворами ТБФ. [14]
Иногда экстракция металлов сопровождается высаливанием ( или всаливанием), как это показано на рис. 9.10 на примере экстракции урана ( У1) из нитратных сред раствором ТЛА в о-ксилоле. Удовлетворительного объяснения этих явлений пока не существует. [15]
Страницы: 1 2