Нитратная среда
Cтраница 2
Иногда экстракция металлов сопровождается высаливанием ( или всаливанием), как это показано на рис, 9.10 на примере экстракции урана ( УТ) из нитратных сред раствором ТЛА в о-ксилоле. Удовлетворительного объяснения этих явлений пока не существует. [16]
В этом методе сочетается отделение нептуния от посторонних металлов с помощью нитратного элюирования и отделение от других актиноидов с помощью хлоридного элюирования, а также замена нитратной среды на хлорид-иую. [17]
Было выяснено, что гидролизованные катионы металлов лучше всего извлекаются из нитратных сред, плохо из сульфатных. Из нитратных сред хорошо извлекаются висмут ( III), железо ( III), медь, кобальт, цинк, никель, хуже цирконий и гафний. Состав экстрагируемых комплексов был установлен, как непосредственным химическим анализом, так и методом сдвига равновесия. [18]
При использовании нитратной среды вместо хлоридной наблюдается целый комплекс мешающих влияний. [19]
Для выделения технеция из производственных растворов и его очистки широкое применение получили такие экстрагенты, как амины и кетоны. Экстракция технеция пиридином из щелочных нитратных сред позволяет не только практически количественно, но и селективно извлекать технеций. Это видно из табл. 15 и 18, в которых приведены коэффициенты распределения технеция и некоторых других продуктов деления урана при экстракции этим реагентом. [20]
Скандий также экстрагируется трибутилфосфатом из нитратной среды. [21]
Показана возможность применения триалкиламинов [267, 354, 834-836], а также нитратов ЧАО [836, 837, 844] для выделения этих элементов из нитратных растворов. Некоторые данные о закономерностях экстракции трехвалентных актиноидов из нитратных сред приведены в гл. Из этих данных следует, что при экстракции из насыщенных нитратами растворов с ограниченной концентрацией HNO3 трехвалентные актиноиды могут быть извлечены и отделены от многих примесей. Показано [406], что высокая а -, Р - и у-активность перерабатываемого материала не оказывает заметного вредного действия на свойства растворов ЧАО в ксилоле. [22]
Серьезным недостатком капающего ртутного электрода является относительно легкая окисляемость ртути. По этой причине ртуть не всегда можно использовать в качестве анода; в нитратной среде окисление происходит при потенциале, большем чем 0 3 В относительно нас. В присутствии анионов, образующих со ртутью нерастворимые соли или устойчивые комплексы, анодное растворение происходит при менее положительном потенциале. Например, в одномольном растворе цианида натрия ртуть окисляется при потенциале около - 0 78 относительно нас. [23]
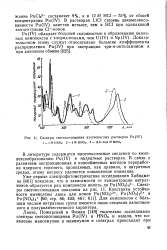 |
Спектры светопоглощения азотнокислых растворов Pu ( IV. [24] |
В литературе содержатся многочисленные сведения по комп-лексообразованию Pu ( IV) в нитратных растворах. В связи с развитием экстракционных и ионообменных методов переработки ядерного горючего, проводимых, как правило, в нитратных средах, этому вопросу уделяется повышенное внимание. [25]
В работе [92] показано, что молибден ( VI) восстанавливается на капающем ртутном электроде в разбавленной HNO3, содержащей молочную и щавелевую кислоты. Описан высокочувствительный метод определения молибдена по каталитической волне восстановления водорода в азотной или хлорной кислоте. В работе [94] в нитратной среде достигнута чувствительность определения молибдена 0 005 мкг / мл. [26]
На том же принципе основаны быстрые методы отделения меди от свинца [70 ] и от олова и сурьмы [81 ] в растворе тартрата аммония. Некоторые разделения, в которых также применяются органические комплексообразующие реагенты, основаны на том, что оксалатные комплексы цинка и кадмия менее прочны, чем соответствующие комплексы других элементов, в частности, меди [19] и урана. Изучались также условия разделения цинка и кадмия в нитратной среде [30]; наилучшие результаты получаются при рН 4 ( ср. [27]
Титрование следует проводить в нейтральной среде, так как повышение кислотности даже до 0 002 М приводит к заметному растворению осадка. Нежелательна также уксуснокислая среда, так как она способствует образованию малодиссоциированного ацетата кальция, что также вызывает занижение результатов титрования. Вполне удовлетворительные результаты получаются при титровании в хло-ридной или нитратной среде. [28]
Страницы: 1 2