Сродство - катион
Cтраница 1
Сродство катионов к полимеру тем больше, чем больше заряд, так как с повышением заряда возрастает чи-слхз связей этих ионов с радикалом ионита. [1]
Уменьшение сродства катиона к водной фазе и большой молекулярный вес органических аддендов облегчают возможность извлечения металла из водной в органическую фазу. [2]
В силу неодинакового сродства собственных катионов и анионов к поверхности кристалла такие частицы оказываются заряженными и в растворах, не содержащих избытка одного из собственных ионов кристалла. Отсюда следует, что причинами возникновения заряда на поверхности частицы ( а следовательно и скачка потенциала на границе частица - раствор) в общем случае являются различие сил, удерживающих катионы и анионы на поверхности кристалла, и неодинаковое взаимодействие их с частицами растворителей. [3]
Прочность связей, степень сродства катионов металлов к функциональным химическим группировкам в организме, также может определять не только общую токсичность, но избирательность ила специфичность действия. [4]
Прочность связей, степень сродства катионов металлов к функциональным химическим группировкам в организме, также может определять не только общую токсичность, но избирательность или специфичность действия. [5]
Иначе говоря, чем сильнее сродство катиона к электронам, тем легче осуществляется отрыв их от аниона О2 - и тем менее устойчив окисел. Примером этого может служить также и тот факт, что высшие окислы и сульфиды одного и того же металла диссоциируют легче, чем низшие. Известно, что потенциал ионизации для отрыва последующего электрона всегда больше, чем для предыдущего. [6]
Не обнаружено никакой корреляции между сродством катиона к поверхности стекла и электродной функцией стеклянной мембраны по отношению к этому катиону. Функция определяется главным образом подвижностью ионов в гелевом слое. [7]
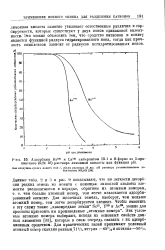 |
Адсорбция Ваш и La14 ( J амберлитом Ш-1 в Н - форме из 5-процентного ( 0 24 М раствора лимонной кислоты как функция рН. [8] |
Это можно объяснить тем, что сродство катионов к иониту является функцией радиуса гидратированного иона, тогда как прочность комплексов зависит от радиусов негидратированных ионов. [9]
Более подробные сравнительные исследования показали, что сродство катионов к ряду ионообменников аналогично или идентично так называемому лиотропному ряду. [10]
В связи с таким первичным механизмом действия металлов особое значение должны иметь как избирательное сродство катиона металла к тем или иным рецепторам - анионным группам на поверхности или внутри клетки, так и сила образующихся при их взаимодействии связей, иначе говоря, прочность возникающих комплексов. [11]
В связи с таким первичным механизмом действия металлов особое значение должны иметь как избирательное сродство катиона металла к тем или иным рецепторам - анионным группам на поверхности или внутри клетки, так и сила образующихся при их взаимодействии связей, иначе говоря, прочность возникающих комплексов. [12]
Процесс кинетического обмена ионов между поверхностью кристалла и раствором приводит также к отклонению состава поверхностного слоя от стехиометрического соотношения вследствие неодинакового сродства собственных катионов и анионов к поверхности кристалла и к возникновению на поверхности кристалла свободного электрического заряда. [13]
Во-первых, константа обмена зависит от соотношения в константах / Сд ( в) а - й Kpjw, которые определяются энергией сродства катионов или анионов к ионогенным группам. Различие в энергии сродства особенно велико при обмене одновалентного иона на двухвалентный, при замене иона, имеющего оболочку инертного газа, на сильно поляризуемый ион, не имеющий оболочки инертного газа, например при обмене ионов натрия на ионы серебра. [14]
Сольватация аполярной части иона сдвигает ионообменное равновесие в сторону уменьшения Ки вследствие ослабления дисперсионного взаимодействия углеводородного радикала с матрицей, а также благодаря усилению сродства катиона к бинарному раствору. Резкое уменьшение величины Ки при малых добавках метанола согласуется с представлениями работ [5-7], в которых указывается, что молекулы неэлектролита, а также ионы электролита располагаются главным образом в пустотах структуры воды. [15]
Страницы: 1 2