Сродство - атом
Cтраница 2
Степень сродства атомов галогенов к электрону сильно сказывается и при образовании кислородных соединений. И действительно, реакция окисления, состоящая в отрыве электронов из внешней электронной оболочки атомов галогенов, протекает легче с бромом и йодом, чем с хлором. Кислородные соединения йода более стойки, чем такие же соединения брома и хлора. Получить кислородные соединения фтора очень трудно даже косвенным путем. [16]
Будет ли сродство атома к электрону равно по величине потенциалу ионизации аниона этого атома. [17]
А - сродство атома кислорода к электрону; ф - работа выхода; D - энергия диссоциации молекулы кислорода; W - энергия взаимодействия образовавшегося иона с катализатором; эта величина должна зависеть от положения адсорбированной частицы на поверхности и пока не может быть определена в рамках элементарных зонных теорий. [18]
Число единиц сродства атома N равно трем. [19]
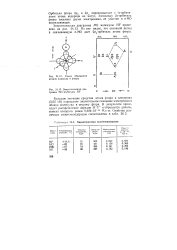 |
Схема сближения атомов водорода и фтора.| Энергетическая диаграмма МО молекулы HF.| Характеристики галогеноводородов. [20] |
Большое значение сродства атома фтора к электрону ( 3 62 эВ) определяет значительное смещение электронного облака молекулы в сторону фтора. [21]
Изменение степени сродства атомов галогенов к валентным электронам сказывается и в реакциях вытеснения одного галогена другим. Так, фтор легко вытесняет хлор, бром и иод из их соединений с водородом или металлами; хлор вытесняет только бром и иод ( но не фтор), а бром в состоянии вытеснить только иод. [22]
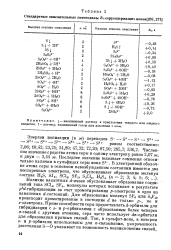 |
Стандартные окислительные потенциалы JSo серусодержащих ионов. [23] |
Численное значение сродства атома серы к одному электрону равно 2 07 эв, к двум - 3 44 эв. [24]
Что называют сродством атома к электрону. Для каких элементов эта величина имеет наибольшее положительное значение и для каких отрицательное значение. Какие экспериментальные данные указывают на невозможность существования многозарядных простых ионов. [25]
В зависимости от сродства атомов к электрону вероятность пребывания электронов в поле ядер разных атомов неодинакова, и поэтому средняя плотность электронного облака у одного атома больше, чем у другого. [26]
Здесь 4 единицы сродства атома углерода насыщены 4 атомами водорода. У второго парафина - этана С2Н6 - 2 атома углерода связаны между собой, а свободные 6 единиц связи насыщены 6 атомами водорода. Дальше мы имеем С3Й8, С4Ню - словом, по алгебраической формуле С Н2л 2 так что, прибавляя каждый раз группу СЬЬ, мы получаем тело, качественно отличное от предыдущего. Какое качественное различие приносит с собой количественное прибавление СзНв, можно узнать на основании опыта: достаточно принять в каком-нибудь пригодном для питья виде, без примеси других алкоголей, винный спирт С2Н0О, а в другой раз принять тот же самый винный спирт, но с небольшой примесью амилового спирта С5Н12О, являющегося главной составной частью гнусного сивушного масла. [27]
Соответственно с повышением сродства атомов элементов к валентным электронам возрастает стойкость металлов к окислению, уменьшается прочность окислов и их гидроокисей. У алюминия, цинка, свинца и других появляются амфотерные свойства. Другими словами, эти элементы, наряду с металлическими, проявляют и ряд металлоидных свойств. Например, алюминий образует А1 ( ОН) 3 - вещество, являющееся одновременно слабым основанием и слабой кислотой. [28]
Окислительно-восстановительный потенциал обусловлен сродством атома к электронам. Заряд же всего иона в целом почти не играет роли. [29]
От энергии ионизации и сродства атома к электрону зависит электроотрицательность ( ЭО) - способность атома данного элемента к оттягиванию на себя электронной плотности по сравнению с другими элементами соединений. ЭО представляет собой полусумму ПИ и СЭ. Расположение элементов в ряду по электроотрицательности закономерно и служит для объяснения химической связи в молекулах и соединениях. [30]
Страницы: 1 2 3 4