Сродство - фермент
Cтраница 2
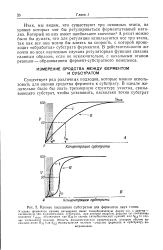 |
Кривые насыщения субстратом для ферментов двух типов. [16] |
Существует ряд различных подходов, которые можно использовать для оценки сродства фермента к субстрату. [17]
Хотя химическое строение таких промежуточных соединений еще не известно, но измерения сродства фермента к субстра7У и к продуктам распада субстрата позволили сделать ряд выводов. Оказалось, например, что скорость распада сахарозы в каждый данный момент пропорциональна концентрации нестойкого соединения с ней фермента. Для каталазы удалось непосредственно наблюдать не только образование промежуточного соединения фермента с перекисью метилового спирта, но и распад этого соединения. Оказалось, что степень диссоциации соединения фермент субстрат определяет скорость ферментной реакции. [18]
В отличие от Vmax, на которую концентрация солей оказывает незначительное влияние, кажущееся сродство фермента к субстрату резко меняется при изменении концентрации соли. [19]
В работе приходилось использовать более высокие концентрации синтетических аналогов производных кофермента А, поскольку сродство ферментов к этим аналогам было несколько меньше - возможно, из-за отсутствия некоторых групп, облегчающих взаимодействие кофермента А с ферментами. [20]
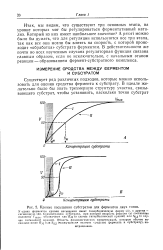 |
Кривые насыщения субстратом для ферментов двух типов. [21] |
Область физиологических концентраций, которые обычно несколько ниже К или SQ 5 ( кажущихся величин сродства фермента к субстрату), заштрихована. [22]
 |
Возможные компоненты системы, включающей фермент, ингибитор. [23] |
Если устойчивость тройного комплекса ELI близка к устойчивости двойного EI, связывание ингибитора I не влияет на сродство фермента к иммобилизованному ли-ганду и присутствие ингибитора не влияет на удерживание фермента. [24]
Истолкование этих фактов затруднительно не только из-за множественности функций витамина В6, но также ввиду неодинаковой степени сродства различных пиридоксалевых ферментов к коферменту. Интересно отметить, что при определенных условиях возможен рост бактерий в отсутствие добавленного витамина В6; однако не исключена возможность синтеза небольших количеств витамина микроорганизмами. [25]
Наряду с различиями в зарядах фермента и фермент-субстратного комплекса на эффективность элюирования влияют также сила связи между ферментам и ионообменником и сродство фермента к аффинному лиганду. [26]
 |
Определение Км и Vmsx методом двойных обратных величин.| Определение Км и Vm, методом Эди-Хофсти. [27] |
Константа Михаэлиса имеет большое значение при исследовании ферментов; она является весьма важным параметром, характеризующим, в частности, степень сродства фермента к субстрату. [28]
Так как высшие уровни структуры белков поддерживаются слабыми связями тех же типов, что и фермент-субстратные комплексы, изменения температуры могут влиять на сродство фермента к субстрату, изменяя геометрию связывающего субстрат участка. [29]
Активация фосфодиэстеразы при действии комплекса Са2 - КМ сопровождается увеличением величины I / max от 3 до 50 раз и уменьшением эффективной константы сродства фермента к субстрату не более чем в 5 раз в зависимости от способа очистки и времени хранения фермента. Взаимодействие антагонистов кальмодулина возможно не только с каль-модулином, но и с фосфодиэстеразой, однако последний эффект обычно не учитывают, так как он появляется при значительно более высоких концентрациях антагонистов, чем первый. [30]
Страницы: 1 2 3 4