Сродство - фермент
Cтраница 3
Какой-то обходный путь здесь необходим из-за двух особенностей этого этапа: во-первых, в прямом направлении ( при гликолизе) эта реакция протекает с большим изменением свободной энергии ( - 4 5 ккал / моль) и, во-вторых, сродство фермента к 1 3-дифосфоглицерату более чем в 100 раз выше, нежели к 3-фосфоглицерату. Поэтому, хотя in vitro и можно заставить эту реакцию идти в обратном направлении, in vivo такой кинетический обход, вероятно, был бы физиологически неэффективным, если даже он и осуществим. [31]
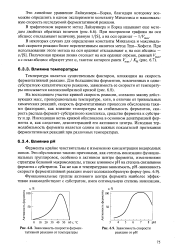 |
Зависимость скорости ферментативной реакции от температуры.| Зависимость скорости реакции от рН. [32] |
На восходящем участке кривой скорость реакции, согласно закону действующих масс, пропорциональна температуре, хотя, в отличие от тривиальных химических реакций, скорость ферментативных процессов обусловлена такими факторами, как влияние температуры на стабильность ферментов, скорость распада фермент-субстратного комплекса, сродство фермента к субстрату и др. Нисходящая ветвь кривой обусловлена в основном денатурацией фермента и, как следствие, дезинтеграцией его активного центра. Исходная термолабильность фермента является одним из важных показателей протекания ферментативных реакций при различных температурах. [33]
Очищенный фермент катализирует также окисление L-молочной кислоты в пировиноградную и глиоксилевой кислоты в щавелевую. Сродство фермента к этим субстратам уменьшается в следующем порядке: гликолевая кислота, молочная, глиоксилевая. [34]
Кинетический параметр ферментативной реакции, численно равный концентрации субстрата, при которой скорость реакции составляет половину максимальной. Характеризует сродство фермента к субстрату. [35]
Концентрация субстрата, при которой достигается скорость, равная половине максимальной, обозначается / См и называется константой Михаэлиса. Константа Михаэлиса характеризует сродство фермента к субстрату: чем больше эта величина, тем больше сродство, и наоборот. [36]
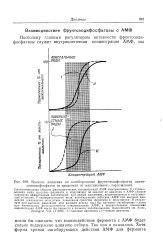 |
Влияние давления на ингибирование фруктозодифосфатаз адено. [37] |
Приблизительная область физиологических концентраций АМФ заштрихована. У глубоководного вида сродство фермента к модулятору не зависит от давления и АМФ служит одинаково эффективным ингибитором при любых давлениях, встречающихся в естественных условиях. У поверхностного вида ингибирующее действие АМФ при высоких давлениях усиливается вследствие повышения сродства фермента к модулятору. В результате при высоких давлениях этот фермент всегда был бы частично ингибирован - даже при наименьших физиологических концентрациях АМФ, а незначительное повышение концентрации АМФ могло бы привести к полному ингибированию. [38]
Таким образом, при использовании иммобилизованной аминоацилазы можно данный процесс проводить многократно и получать свободные L-аминокислоты с максимальным выходом. Оказалось, что сродство фермента к ацилированным аминокислотам примерно одинаково и определяется не строением аминокислоты как таковой, а исключительно ацильной группировкой. [39]
Трудно установить, какая именно оксидаза катализирует поглощение кислорода in vivo. В этом отношении показательно сродство ферментов к кислороду. Высоким сродством к кислороду обладает цитохромоксидаза. У большинства других оксидаз оно невелико; можно ожидать, что при нормальном парциальном давлении кислорода их активность будет низкой. [40]
Для чего нужны столь высокие концентрации РуДФ - карбо-ксилазы. Такое огромное несоответствие между сродством фермента к субстрату и физиологическими концентрациями субстрата встречается крайне редко. Понятно, что для эффективной работы РуДФ - карбокси-лазы при условиях, столь далеких от полного насыщения, может потребоваться поддержание необычно высоких концентраций фермента. [41]
Отрицательная температурная модуляция имеет важное биологическое значение. Одновременное уменьшение кинетической энергии и сродства фермента к субстрату приводит к стремительному падению каталитической активности фермента. В таких условиях Qio может возрастать до огромных величин ( табл. 19); при этом, как и следовало ожидать, температурный коэффициент увеличивается с уменьшением концентрации субстрата. [43]
Величины Р5о, подобно / ( л и 50 5, обычно того же порядка, что и концентрации газа ( или субстрата) в среде, окружающей активный белок. Так же как и параметры сродства ферментов к субстратам, величина А о необычайно чувствительна к изменению физического и химического состояния клеточной среды. [44]
Приведенные здесь кривые иллюстрируют ряд важных особенностей адаптации НЬ. I) Так же как и сродство ферментов к субстратам, величина Р5 находится под сильным давлением отбора, направленного на то, чтобы гемоглобин присоединял и отдавал Ог при соответствующих условиях. У высокоактивных видов величины Рго обычно выше, чем у менее подвижных форм. Абсолютная величина сродства НЬ к Ог может также отражать концентрацию кислорода в обычной для данного организма среде. Мы видим, например, что у антарктических рыб, обитающих в насыщенной кислородом холодной ( - 1 9 С) воде, величины РЗО выше, чем у такой медлительной донной рыбы, как японский угорь ( Anguilla japonica ], который живет в сравнительно бедной кислородом среде. [45]
Страницы: 1 2 3 4