Стабилизация - поливинилхлорид
Cтраница 3
 |
Технологическая схема получении стеарата кальция. 1 - ысрпик. 1 - - реактор. 3 - центрифуга. 4 - аэрофон т анн ал сушилка. [31] |
Технологическое оформление производства обычно не вызывает затруднений, однако специфика применения стеарата кальция для стабилизации поливинилхлорида требует определенных выпускных форм - - стабильных эмульсий, растворов или высокодисперсных порошков. [32]
Кроме перечисленных трех основных типов эпоксидных соединений, в литературе есть данные о применении для стабилизации поливинилхлорида некоторых других веществ, содержащих эпоксидные циклы в молекулах. В качестве стабилизаторов описаны соли свинца, бария, кальция, кадмия и алифатических эпоксикис-лот, с 11 - 22 атомами углерода в цепи. [33]
 |
Схема установки для исследования термического разложения поливинилхлорида. [34] |
В последние годы опубликованы результаты исследований, позволяющих оценить все многообразие превращений при разложении и стабилизации поливинилхлорида. Ток сухого газа ( азот, кислород или воздух), пройдя спиральный подогреватель ( погруженный в масляную баню) со скоростью 150 мл / мин, поступал в нагреваемую трубку, заполненную исследуемым образцом. [35]
Нитрильные каучуки весьма подвержены окислительной деструкции, но несмотря на это они в известной мере содействуют стабилизации поливинилхлорида. [36]
Органические и неорганические соли кальция, бария, кадмия, цинка, свинца, слона находят широкое применение для стабилизации поливинилхлорида. Мировая промышленность производит примерно 150 наименований солей стеариновой, лауриншой, малеино-вой, фталевой, салициловой, угольной, серной, фосфористой и кремневой кислот; насчитывается до 1ГЮО торговых марок индивидуальных солей и более 100 марок смссепых композиций. [37]
Однако сведения о повышении термической стабильности поливинилхлорида путем сополимеризации с небольшими количествами глицидилметакри-лата [ 21 j не могут служить основанием для общей оценки эффективности такого способа стабилизации поливинилхлорида. [38]
После отделения пластификатора, наполнителей и эмульгаторов в остатке определяют стабилизаторы. Для стабилизации поливинилхлорида используют очень большое количество соединений. Особенно часто применяются соли свинца, кадмия, бария, органические соединения олова. [39]
Поскольку скорость термодеструкции поливинилхлорида обратно пропорциональна его молекулярной массе, инициирование, - вероятнее всего, происходит у концов цепей. Возможно, что стабилизация поливинилхлорида бариевыми и кадмиевыми солями карбо-новых кислот заключается з обмене его подвижных атомов хлора на карбоксильные группы стабилизаторов. [40]
Поскольку скорость термодеструкции поливинилхлорида обратно пропорциональна его молекулярной массе, инициирование вероятнее всего происходит у концов цепей. Возможно, что стабилизация поливинилхлорида бариевыми и кадмиевыми солями карбоновых кислот заключается в обмене его подвижных атомов хлора на карбоксильные группы стабилизаторов. [41]
Поскольку скорость термодеструкции поливинилхлорида обратно пропорциональна его молекулярной массе, инициирование, вероятнее всего, происходит у концов цепей. Возможно, что стабилизация поливинилхлорида бариевыми и кадмиевыми солями карбо-новых кислот заключается з обмене его подвижных атомов хлора на карбоксильные группы стабилизаторов. [42]
Паркер [333] показал, что объяснение процесса стабилизации только за счет связывания выделяющегося хлористого водорода несостоятельно; ряд веществ, хорошо связывающих хлористый водород, не стабилизируют поливинилхлорид. По мнению автора, механизм стабилизации поливинилхлорида оловоорганическими соединениями имеет, вероятно, радикальный характер. При использовании в качестве стабилизатора дибутилдиаце-тата олова с С14 в бутильном радикале установлено присоединение бутильных групп к полимеру. [43]
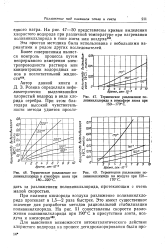
При наличии кислорода воздуха разложение поливинилхлорида протекает в 1 5 - 2 раза быстрее. Это имеет существенное значение для разработки методов рациональной стабилизации поливинилхлорида. [45]
Страницы: 1 2 3 4