Стабилизация - енольная форма
Cтраница 1
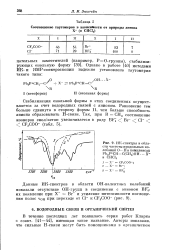 |
ИК-спектры в области частоты продольных колебаний О - Н в комплексах Ph3P CHC ( CH3 OH. X-в СНС13. [1] |
Стабилизация енольной формы в этих соединениях осуществляется за счет водородных связей с анионом. Равновесие тем больше сдвинуто в сторону формы II, чем больше способность аниона образовывать Н - связи. [2]
Напротив, стабилизация енольной формы за счет водородной связи осуществляется в гексане строго внутримолекулярно, в то время как в чистом продукте она может быть частично межмолекулярной, что еще несколько снизит вероятность образования енолыюй формы. [3]
Затем происходит - стабилизация енольной формы путем передачи одного из атомов водорода гем-диола к ос-атому углерода. [4]
Водородная связь такого типа имеет важное значение для стабилизации енольной формы, о чем свидетельствует увеличение содержания енольной формы в растворителях ( например, гексане), которые не могут эффективно сольватировать кетонные группы ке-то-формы. [5]
Образование внутримолекулярной водородной связи, возможно, играет важную роль в стабилизации енольной формы. С этой точки зрения понятно, j почему ацетилацетон примерно на 80 % существует в виде енола. [6]
Необходимо, однако, отметить, что в последнем случае возможна некоторая стабилизация енольной формы за счет водородной связи. Енол 1 3-циклоок-тандиона существует исключительно в транс-форме. [7]
Так как резонанс водородной связи [130] представляет собою стабилизирующее влияние, то он и усиливает стабилизацию енольной формы по сравнению с кето-формой. Таким образом, любой растворитель, затрудняющий внутрикомплексную циклизацию, будет способствовать переходу в кето-форму. Растворитель может производить такое действие двумя различными способами: 1) играя роль донора по отношению к водородному атому гидроксила енольной формы или 2) играя роль акцептора по отношению к кетонному кислородному атому енола. Следовательно, здесь могут проявляться как кислотные, так и основные свойства растворителя, причем в обоих случаях они будут благоприятствовать образованию кетонной формы. Повидимому, этих соображений достаточно для объяснения наблюдаемой последовательности влияний растворителей. Так, вода, будучи наиболее основной, должна быть наиболее эффективной. Продвигаясь далее по списку в табл. 16, мы видим, что все остальные растворители, вплоть до последней апротической пары, находят себе место в последовательности, которая, по всей вероятности, соответствует последовательности их кислотностей, так как следует ожидать, что хлороформ будет проявлять заметные кислотные свойства. [8]
При рассмотрении р-дикарбонильных систем выступают два новых фактора, две характерные черты, которые приводят к стабилизации енольных форм и которые чувствительны к пространственным факторам. Во всяком случае, расстояние О-О укорочено ( 1 44А, если считать с учетом расстояния С-С в ароматических соединениях) и водородная связь должна быть довольно прочной. Если только позволяют пространственные факторы, то енолы всех ациклических Р - дикарбонильных соединений должны иметь плоское строение, чтобы энергия сопряжения была наибольшей, и быть циклическими, чтобы могли образоваться прочные водородные связи. [9]
Так как карбонильная группа энергетически более выгодна, чем енольная, простейшие альдегиды и кетоны ( ацеталь-дегид, ацетон и др.) существуют только в карбонильной форме. Стабилизация енольной формы наблюдается в молекулах дикарбонильных соединений, содержащих группировку - СО-СН2-СО -, находящуюся в таутомерном равновесии с группировкой - С ( ОН) СН - СО - ( см. Ацетоуксусный эфир. [10]
Производные J-дикарбонильных соединений подвержены значительной енолизации. Эта особенность объясняется стабилизацией енольной формы в результате резонанса между карбонилом и сопряженной двойной связью, образующейся вследствие енолизации второй карбонильной группы. Эта стабилизация еще более возрастает вследствие хелатообразования с участием енольного водорода. [11]
Если же учитывать другие факторы, влияющие на эффективность стабилизации, то такие водородные связи приводят к уменьшению полярности енола и повышению степени компактности его молекул по сравнению с менее компактными молекулами кетоформы. Именно поэтому в тех случаях, когда кетон-ная и енольная формы могут быть изолированы, оказывается, что енольная форма, несмотря на наличие гидроксильной группы, имеет обычно более низкую температуру кипения. Влияние водородной связи на преимущественную стабилизацию енольной формы легко видеть из сравнения процентного содержания ацетилацетона XXIV в воде и в несодержащем гидроксильных групп растворителе, например в гексане. [12]
Положение равновесия в таутомерией смеси определяется содержанием каждого из изомеров. Оно изменяется в зависимости от трех факторов: относительной термодинамической устойчивости каждого из таутомеров, температуры смеси и природы растворителя, если он применяется. В таком случае возникает вопрос, каким же образом осуществляется стабилизация енольной формы заместителями для других веществ, которые могут рассматриваться как производные ацетона. Увеличение енолизации, вызываемое введением фенильной группы, с 8 до 30 % показывает, что группа С С - ОН стабилизируется за счет сопряжения с фенильным кольцом. Сравнение этил-3 - кетобутаноата и пентандиона-2 4 показывает, что СОСН3 - группа гораздо более эффективна для стабилизации енольной формы, чем СООС2Н5 - группа. [13]
Положение равновесия в таутомерной смеси определяется содержанием каждого из изомеров. Оно изменяется в зависимости от трех факторов: относительной термодинамической устойчивости каждого из таутомеров, температуры смеси и природы растворителя, если он применяется. В таком случае возникает вопрос, каким же образом осуществляется стабилизация енольной формы заместителями для других веществ, которые могут рассматриваться как производные ацетона. Увеличение енолизации, вызываемое введением фенильной группы, с 8 до 30 % показывает, что группа С С - ОН стабилизируется за счет сопряжения с фенильным кольцом. Сравнение этил-3 - кетобутаноата и пентандиона-2 4 показывает, что СОСН3 - группа гораздо более эффективна для стабилизации енольной формы, чем СООС2Н5 - группа. [14]
Положение равновесия в таутомерией смеси определяется содержанием каждого из изомеров. Оно изменяется в зависимости от трех факторов: относительной термодинамической устойчивости каждого из таутомеров, температуры смеси и природы растворителя, если он применяется. В таком случае возникает вопрос, каким же образом осуществляется стабилизация енольной формы заместителями для других веществ, которые могут рассматриваться как производные ацетона. Увеличение енолизации, вызываемое введением фенильной группы, с 8 до 30 % показывает, что группа С С - ОН стабилизируется за счет сопряжения с фенильным кольцом. Сравнение этил-3 - кетобутаноата и пентандиона-2 4 показывает, что СОСН3 - группа гораздо более эффективна для стабилизации енольной формы, чем СООС2Н5 - группа. [15]
Страницы: 1 2