Стабильность - золи
Cтраница 1
Стабильность золей связана с электрическими свойствами поверхности коллоидных частиц. Золи устойчивы вследствие того, что мицеллы, имеющие электрические заряды одинакового знака, отталкиваются друг от друга, а потому и не слипаются. [1]
Стабильность золей возрастает при повышении диэлектрической постоянной ( е) растворителя. Золи, полученные в растворителях с низкой е ( бензол, ксилол, трипропиламин), нестабильны. Что же касается устойчивых золей, то расположить их по степеням стабильности не представляется возможным из-за протекающего в них процесса металлизации, связанного с истинной растворимостью металла. [2]
Сохранение стабильности золей Сг203 при действии рентгеновских лучей даже после поглощения очень большого количества энергии и некоторое повышение в этих условиях значения С-потенциала без изменения дисперсности золя ( постоянство мутности) можно объяснить тем, что появляющийся шестивалентный хром не остается на поверхности в виде анионных комплексов, которые снижали бы положительный заряд, а десор-бируется и переходит в интермицеллярную жидкость. [3]
Нарушение стабильности золей гидроокисей различных металлов при действии ионизирующих излучений вызывается радиационно-хими-ческими окислительно-восстановительными реакциями, протекающими между стабилизирующими комплексами, находящимися на поверхности частиц, и атомами водорода или радикалами гидроксила, возникающими в интермицеллярной жидкости золя при взаимодействии излучения с водой. [4]
Этим фактором в значительной мере определяется стабильность золей металлов. Но он действует, очевидно, лишь при малых концентрациях, когда столкновения действительно только парные. [5]
Эти авторы считают, что изменение стабильности золей при облучении вызывается взаимодействием первичных ионов, образующихся в интермицелляриой жидкости с зарядами частиц. Так как электроны легче могут приближаться к поверхности частиц, чем ионы, только положительно заряженные золи должны терять стабильность при облучении. Этот вывод находится в противоречии с экспериментальными данными самих авторов. [6]
Простой расчет показывает при этом, что объяснить стабильность настоящих золей только ничтожными размерами отдельных частиц нельзя. [7]
Таким образом, радикал ОН, так же как и солъватиро-ванный электрон, должен уменьшать стабильность положительно заряженных золей и стабилизировать или оставлять неизменными отрицательно заряженные золи. Но, основываясь на такой точке зрения, следует учитывать возможность противоположного эффекта за счет ионов Н, образующихся из атомов водорода. В среде, где гидратированные электроны превращаются в атомы водорода, а последние восстанавливаются в ионы Н, должна наблюдаться под воздействием излучения стабилизация положительно заряженных и коагуляция отрицательно заряженных золей. Возможно, невоспроизводимость результатов, отмеченная выше, связана с такими сложными явлениями. [8]
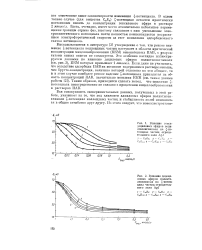 |
Влияние гекса-дециловых эфиров полиэтиленгликоля на. - по-тенциал частиц отрицательного золя AgJ.| Влияние додеци-ловых эфиров полиэтиленгликоля на - потенциал частиц отрицательного золя AgJ. [9] |
Вся совокупность экспериментальных данных, полученных в этой работе, указывает на то, что под влиянием алкиловых эфиров полиэтилен-гликоля - потенциал коллоидных частиц и стабильность золей изменяются в общем антибатно друг другу. [10]
Херд, Раймонд и Миллер [18], а также и другие показали, что соли натрия, как, например, хлорид или нитрат, понижают стабильность золей кремнезема. Следовательно, не является неожиданным, что золи, полученные при взаимодействии кислоты с силикатом натрия, весьма неустойчивы. Описаны два метода отделения кремневой кислоты от электролита, которые основаны на применении органических растворителей. [11]
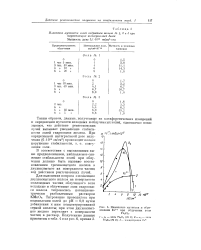 |
Изменение мутности и образование Fe при облучении золя Ге203. [12] |
Таким образом, данные, полученные из катафоретических измерений и определения мутности исходных и облученных золей, однозначно показывают, что действие рентгеновских лучей вызывает уменьшение стабильности золей гидроокиси железа. [13]
Из сравнения приведенных данных по устойчивости золей и сопоставления литературных данных по сорбнруемостп ионов хлора, сульфата и фосфата на двуокиси титана [3. 7-9, 11, 12] видно, что между стабильностью золей и сорбируемостыо анионов существует симбатная зависимость. Аналогичная зависимость имеет место и для катионов. [14]
Катафоретические опыты приводят к следующему представлению о природе изученных коллоидов: на поверхности металлических частиц находятся ионогенные группы, отдающие в наружную обкладку двойного слоя ионы щелочного металла, что обусловливает отрицательный заряд частиц и стабильность золей. [15]
Страницы: 1 2