Стабильность - золи
Cтраница 2
Стабильность золей обусловлена, как мы видели, зарядами адсорбированных ионов Снятие этих зарядов вызывает коагуляцию. В растворах лиофильных коллоидов прибавляется новый фактор, который чаете имеет решающее значение: защита от коагуляции оболочкой воды, окружающей мицеллу. Чтобы вызвать коагуляцию лиофильных коллоидов в виде плотногс осадка, необходимо не только снять заряд с коллоидальных частиц, но еще их дегидратировать. Без дегидратации раствор постепенно застывает в гель. [16]
Золи двуокиси марганца являются типичными ацидоидными золями, как это следует из данных, полученных Иоши и Нарган [2], которые показали, что при коагуляции этих золей различными катионами соблюдается правило валентности. О действии рентгеновского излучения па стабильность золей двуокиси марганца в литературе никаких сведений не имеется. [17]
Специфическая адсорбция многозарядных катионов, таких как А1, ре, может привести к перезарядке поверхности. При отсутствии зарядов в области низких рН стабильность золей обусловлена наличием гидратных оболочек, препятствующих агрегированию частиц между собой. [18]
Золи Мп02 облучались в течение различных промежутков времени. Данные по изменению мутности показывают, что действие рентгеновских лучей вызывает снижение стабильности золей. При интегральной дозе - 3 - 1019 эв / см3 наступает коагуляция. [19]
В трактовке причин изменения устойчивости золей ППК с изменением рН мнения авторов также резко расходятся. Айлер [2] не учитывает связи ИЭТ с устойчивостью и считает причиной максимума стабильности золей ПКК следовые примеси фторид-иона и катионов - комплексообразовате-лей в золях. Ряд авторов [5, 6] полагает, что наиболее устойчивыми золи ПКК должны быть в ИЭТ, так как, по их мнению, появление ионов силиката с ростом рН ускоряет каталитический процесс полимеризации ПКК; эти исследователи оставляют вне поля зрения взаимодействие ПКК с дисперсионной средой - водой. [20]
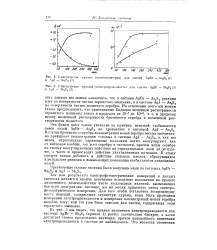 |
Кинетические кривые ( потонциометрия для систем AgBr - As2S3 ( 1. и AgJ - As2S3 ( 2.| Кинетические кривые ( электропроводность для систем AgBr - Sb2S3 ( 1. и AgJ - Sb2S3 ( 2. [21] |
В случае бромистого серебра концентрация ионов серебра весьма значительно превышает концентрацию таковых в системе AgJ - As2S3, а, как мы знаем, отрицательно заряженные коллоиды легко коагулируют как от катионов вообще, так и от серебра в частности, причем ионы серебра по своему коагулирующему действию на отрицательные золи не уступают, а часто и превосходят действие двухвалентных катионов. К этому следует также добавить и действие сильных кислот, образующихся в результате реакции и вызывающих понижение стабильности ацидоидных золей. [22]
Как видно из приводимых ниже данных, скорости хорошо очищенных металлизирующихся золей значительно ниже, чем защищенных золей. Слишком большое количество окиси металла, обыкновенно присутствующее при первых перегонках, не только не повышает, но и снижает катафо-ретическую скорость и вместе с тем стабильность золей. Так, при первой перегонке часто наблюдается выпадение геля. [23]
Эфирозоли натрия, розовато-желтые в отраженном и фиолетовые в проходящем свете, не отличаются существенно от золей калия. Частицы их заряжены отрицательно. Скорость несколько выше, стабильность их значительно превосходит стабильность золей калия. [24]
Для пропиламина приведены числа, относящиеся к изопропиламину. Дипольный момент и диэлектрическая постоянная для трипропиламина получены экстраполяцией из данных, относящихся к триметиламину и триэтиламину. Из небольшого количества приведенных данных нельзя, конечно, сделать какие-либо заключения о влиянии дипольного момента молекул растворителя и концентрации их в растворе на стабильность золей. Этот вопрос должно выяснить специальное исследование. [25]
В предыдущем сообщении [1] было показано на примере положительных золей окисей металлов, что стабильность может нарушаться или сохраняться без изменений при действии рентгеновского излучения, в зависимости от того, способны ли стабилизирующие комплексы, находящиеся на поверхности частиц, участвовать в окислительно-восстановительных реакциях за счет атомов Н и радикалов ОН, возникающих в воде. Именно протекание таких реакций, возможное, если металлы, входящие в состав комплексов, обладают переменной валентностью, влечет за собой изменение заряда поверхности. В настоящей статье приводятся новые данные, полученные как с положительными, так и с отрицательными золями, подтверждающие правильность представлений, согласно которым изменение стабильности золей при действии излучения определяется только радиационно-химическими реакциями на поверхности частиц и не зависит от знака их заряда. [26]
Высокомолекулярные соединения и лиофильные коллоиды являются стабилизаторами по отношению к лиофобным золям. Так, если прибавить к раствору соли серебра небольшое количество желатина, белка ( или некоторых продуктов распада его) и восстановить серебро до образования золя, то степень дисперсности коллоидного серебра в этих условиях получения оказывается более высокой и золь менее - подвержен влияниям факторов, вызывающих коагуляцию. Такой золь серебра можно путем выпаривания превратить в твердый продукт, который обладает способностью снова растворяться в воде, образуя золь. Вследствие защитного действия, которое в подобных случаях оказывают лиофильные коллоиды, повышая стабильность необратимых золей, их называют защитными коллоидами. При применении защитных коллоидов звли могут быть получены с более высокимл концентрациями, чем обычно. Примером концентрированного золя, получаемого с применением защитного коллоида, является медицинский препарат колларгол, содержащий более 70 % серебра. [27]
Высокомолекулярные соединения и лиофильные коллоиды являются стабилизаторами по отношению к лиофобным золям. Так, если прибавить к раствору соли серебра небольшое количество желатина, белка ( или некоторых продуктов распада его) и восстановить серебро до образования золя, то степень дисперсности коллоидного серебра в этих условиях получения оказывается более высокой и золь менее подвержен влияниям факторов, вызывающих коагуляцию. Такой золь серебра можно путем выпаривания превратить в твердый продукт, который обладает способностью снова растворяться в воде, образуя золь. Вследствие защитного действия, которое в подобных случаях оказывают лиофильные коллоиды, повышая стабильность необратимых золей, их называют защитными коллоидами. При применении защитных коллоидов золи могут быть получены с более высокими концентрациями, чем обычно. Примером концентрированного золя, получаемого с применением защитного коллоида, является медицинский препарат колларгол, содержащий более 70 % серебра. [28]
Страницы: 1 2