Стабильность - молекула
Cтраница 1
Стабильность молекулы зависит от химических связей ее атомов. Как упоминалось раньше, именно квантовая физика пролила свет на первоначально весьма туманную природу химических связей. Кристалл ( подобный алмазу) является регулярным расположением атомов ( атомов углерода в случае алмаза), периодическим в трех независимых пространственных направлениях. Здесь связи распространяются между всеми атомами, и таким образом кристалл является единственной молекулой. Стабильность твердых тел является стабильностью кристаллов, и если модель Дельбрука в основном верна, то стабильность генов основывается на тех же квантовомеханических основах. Однако, в то время как в кристалле те же самые строительные кирпичи повторяются периодически, каждый атом в гене имеет свои специфические неизменяемые место и роль. Однако Шредингер говорит о гене как об апериодическом кристалле и приписывает ему высшую степень порядка и организации, чем у периодического кристалла. [1]
Стабильность молекулы к электронному удару зависит от ее строения. Так, например, из приведенных ниже данных видно, что замыкание алифатической цепи в цикл значительно больше стабилизирует молекулу, чем простая кратная связь. Наличие же ароматической системы делает молекулярный ион более устойчивым по сравнению с непредельным углеводородом, имеющим открытую цепь. [2]
Стабильность молекул и комплексов меняется в широких пределах. Некоторые комплексы, такие, например, как AlFe в криолите, могут быть более устойчивыми. [3]
Стабильность молекул и комплексов меняется в широких пределах. [4]
Стабильность молекул РНК может варьировать в широких пределах. [5]
Резонанс увеличивает стабильность молекулы и уменьшает выход свободной энергии, высвобождающейся при, гидролизе. [6]
Вследствие этого стабильность молекулы не зависит от размеров цикла. [7]
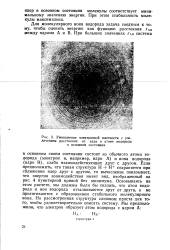 |
Уменьшение электронной плотности с увеличением расстояния от ядра в атоме водорода в основном состоянии. [8] |
При этом стабильность молекулы максимальна. [9]
Представление о стабильности внутриклеточных молекул белка, противопоставляемое идее о том. Моно и сотрудники [600, 601] исследовали индуцированный синтез р-галактозидазы в растущих клетках Escherichia coll. При выращивании на сравнительно простой среде, содержащей соли и янтарную кислоту, эти микроорганизмы не синтезируют заметных количеств р-галактозидазы. [10]
В классической теории стабильность молекулы обеспечивается наличием неразорванной цепи химических связей ( цепи химического действия), снижающих энергию молекулы по сравнению с энергией совокупности свободных бесконечно удаленных атомов. Сопоставляя условия существования системы в виде единой стабильной частицы в квантовой механике и классической теории, можно установить определенное соответствие. [11]
Поскольку существование и стабильность молекулы как единой частицы зависит от наличия и стабильности отдельных отношений непосредственной химической связи между ее атомами, постольку эти отдельные отношения также с полным правом могут быть охарактеризованы с их энергетической стороны. [12]
Последние не повышают стабильности молекулы и вводятся только вследствие математического формализма метода [ там же, стр. Структуры, в которых все связи эффективные, суть невозбужденные структуры, а степень возбужденности структуры определяется числом имеющихся в ней неэффективных связей ( см. далее, стр. [13]
Для того чтобы сравнивать стабильность молекул с разным числом атомов, нужно иметь эталонные системы. Сложности, связанные с выбором таких систем, очевидны, так как соответствующие разности я-электронных энергий должны коррелировать с экспериментальными данными о стабильности сопряженных углеводородов. Проблема выбора эталонной я-электронной системы имеет тесную связь с проблемой ароматичности в органической химии, с попытками найти количественные критерии оценки степени ароматичности углеводородных или гетероатомных сопряженных молекул. [14]
Одной из величин, определяющих стабильность молекулы и самую возможность ее существования как устойчивой, единой частицы, является энергия ее образования из атомов. [15]
Страницы: 1 2 3 4