Стабильность - пересыщенный раствор
Cтраница 1
Стабильность пересыщенных растворов характеризуется предельным пересыщением A6 ft - Ьн. При достижении раствором предельного пересыщения ( лабильная область) происходит спонтанное образование кристаллов. [1]
Стабильность пересыщенных растворов возрастает от I группы к VI, в пределах каждой группы - в последовательности расположения солей. [2]
Если говорить о стабильности пересыщенных растворов данного вещества вообще, нужно иметь в виду два фактора: степень пересыщения и время, в течение которого пересыщенный раствор может находиться без видимых изменений. Они и являются основными критериями устойчивости. Что касается пересыщения, то речь идет не о любом, а о так называемом предельном пересыщении. Предельным пересыщением раствора называется то, выше которого он сразу же начинает кристаллизоваться. Однако чаще при описании пересыщенных растворов используется первое из них. К тому же оно более подходит для оценки устойчивости неравновесных растворов. Знания только величины предельного пересыщения недостаточно для полной характеристики степени устойчивости. Имея близкие предельные пересыщения, вещества между тем могут образовывать растворы различной степени устойчивости. Это различие выражается в том, что при более низких, чем предельное, пересыщениях они могут находиться в метастабильном состоянии неодинаковое время. В качестве примера можно привести водные растворы нитратов стронция и бария, предельные относительные пересыщения для которых при 0.8 С очень близки, а время нахождения в метастабильном состоянии при [ J ниже предельного резко отлично. Поэтому для характеристики устойчивости необходим второй фактор - время. [3]
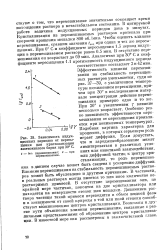 |
Зависимость индукционных периодов от пересыщения для кристаллизации азотнокислого бария при 30 С. [4] |
Эффективность влияния перемешивания на стабильность пересыщенных растворов уменьшается, судя по рис. 37 - 39, с увеличением температуры и снижением пересыщения, причем при 30 в исследованном интервале концентрации действие перемешивания примерно одно и то же. При 20 с увеличением if влияние несколько возрастает. Особенно резко зависимость эффективности перемешивания от пересыщения проявля-ется при пониженных температурах. Подобная картина характерна для процессов, в которых серьезную роль играет диффузия. Если допустить, что и зародышеобразование может лимитироваться в различных условиях или кинетикой взаимодействия, или диффузией частиц к центру кристаллизации, то роль перемешивания в данном случае может быть сведена к ускорению диффузии. Влияние перемешивания на стабильность перемешиваемых растворов может быть обусловлено и другими причинами. В частности, в реальных растворах всегда имеется то или иное количество нерастворимых примесей. В отсутствие перемешивания они, по крайней мере частично, покоятся на дне кристаллизатора или находятся на поверхности стенок или мешалки. Движением раствора частицы такой примеси переводятся в объем жидкой фазы и в зависимости от своей природы в той или иной степени способствуют возникновению центров кристаллизации. Возможны и другие пути объяснения влияния перемешивания, связанные с различными представлениями об образовании центров кристаллизации. В известной мере они рассмотрены в заключительной главе. [5]
Гопала и Растоги [3], стабильность пересыщенных растворов в присутствии ПАВ уменьшается. [6]
Во всех этих исследованиях особое внимание уделяется стабильности пересыщенных растворов и их свойствам. Именно этим вопросам посвящены и основные главы публикуемой книги. Кроме того, автор счел полезным дать небольшое приложение, содержащее данные о предельных пересыщениях и переохлаждениях растворов, полученные разными исследователями. И хотя на сегодня нет единых методов определения этих величин, приведенные значения, на наш взгляд, могут быть использованы в качестве первого ориентира. [7]
Прежде всего следует остановиться на самом понятии стабильности пересыщенного раствора. Шлыковым и Горбачевым [2], а также Товбиным и Красновой [3] за меру стабильности пересыщенных растворов принимается то относительное пересыщение, начиная с которого сразу же наступает спонтанная кристаллизация. Другими словами, мерой стабильности раствора является то предельное пересыщение, при котором латентный период кристаллизации [5] равен нулю. Указанные факторы непосредственно с природой кристаллизующегося вещества не связаны, особенно первый из них, влияние которого на экспериментально получаемые значения предельного пересыщения наиболее существенно. Если учесть, что степень очистки раствора является величиной относительной ( она может быть лучше или хуже, но не может быть полной), то и сами величины предельных пересыщений естественно считать тоже относительными. Стало быть, можно ожидать, что если произвести более глубокую очистку кристаллизуемых веществ и растворителей, то будут получены еще большие величины. Таким образом, проблема оценки стабильности растворов выглядит более сложной, чем это казалось. Она, видимо, не может быть решена только путем наблюдения за началом спонтанной кристаллизации солей в процессе охлаждения их растворов. К тому же следует отметить, что проведение экспериментов при больших пересыщениях всегда сопряжено с большими ошибками. В меньшей степени от чистоты исходных веществ зависит кристаллизация при сравнительно небольших пересыщениях, при которых длительность латентных периодов выражается по крайней мере в часах. Поскольку протяженность этих периодов связана с пересыщением [5], путем экстраполяции могут быть определены значения пересыщений, при которых кристаллизации начинается мгновенно, и те, при которых она практи чески совсем не идет. [8]
Из всего вышесказанного следует, что проблема стабильности пересыщенных растворов требует для своего решения, во-первых, специальных методических разработок, во-вторых, вовлечения в круг исследований большего числа объектов и, в-третьих, создания теории о связи стабильности с составом раствора. [9]
Уравнение (V.7) также может быть использовано для оценки степени стабильности пересыщенных растворов [11 ] и определения растворимости веществ кинетическим методом. Оценка степени стабильности растворов с помощью (V.7) производится следующим способом. Изучается продолжительность индукционных периодов при различных пересыщениях. Обычно она имеет вид прямой. Так как предельное значение индукционного периода в области больших s зависит только от физических характеристик растворимого вещества и растворителя, следует отыскивать такие s, при которых оно достигается. Но практически это не всегда можно сделать из-за невозможности точно определить предельные tind. При решении конкретных инженерных задач вполне достаточно находить коэффициенты пересыщения, отвечающие значениям tind 1 мин. [10]
Кинетика кристаллизации карбоната кальция, как и других солей, зависит также от присутствия примесей [15], которые кроме модификации формы кристаллов могут изменять степень стабильности пересыщенного раствора и скорость кристаллизации в широких пределах. [11]
Большое значение с точки зрения кинетики осаждения имеют сведения об устойчивости пересыщенных растворов и величинах предельных пересыщений и переохлаждений. Стабильность пересыщенных растворов находится в прямой связи с фазообразо-ванием. Чем труднее образуются центры кристаллизации, тем устойчивее раствор. Тут действуют одни и те же причины, определяющие и то, и другое. Следовательно, исследования по устойчивости пересыщенных или переохлажденных растворов одновременно дают возможность глубже понять механизм образования новой фазы. Предельные пересыщения растворов находятся в прямой связи со свойствами растворенных веществ, что дает возможность одновременно судить и о возможных особенностях осадков. Исследования по пересыщенным растворам являются неотъемлемой частью решения проблемы об основных закономерностях зародышеобразования. [12]
В присущих производственным условиям многокомпонентных системах изменяются количественные характеристики всех стадий кристаллизации. Прежде всего изменяется растворимость сахара и степень стабильности пересыщенных растворов. Происходящие изменения сказываются в первую очередь на образовании центров кристаллизации, что в конечном итоге видоизменяет кинетику всего процесса образования осадка. Далее, скорость кристаллизации сахара в присутствии других компонентов тоже оказывается иной. [13]
Прежде всего следует остановиться на самом понятии стабильности пересыщенного раствора. Шлыковым и Горбачевым [2], а также Товбиным и Красновой [3] за меру стабильности пересыщенных растворов принимается то относительное пересыщение, начиная с которого сразу же наступает спонтанная кристаллизация. Другими словами, мерой стабильности раствора является то предельное пересыщение, при котором латентный период кристаллизации [5] равен нулю. Указанные факторы непосредственно с природой кристаллизующегося вещества не связаны, особенно первый из них, влияние которого на экспериментально получаемые значения предельного пересыщения наиболее существенно. Если учесть, что степень очистки раствора является величиной относительной ( она может быть лучше или хуже, но не может быть полной), то и сами величины предельных пересыщений естественно считать тоже относительными. Стало быть, можно ожидать, что если произвести более глубокую очистку кристаллизуемых веществ и растворителей, то будут получены еще большие величины. Таким образом, проблема оценки стабильности растворов выглядит более сложной, чем это казалось. Она, видимо, не может быть решена только путем наблюдения за началом спонтанной кристаллизации солей в процессе охлаждения их растворов. К тому же следует отметить, что проведение экспериментов при больших пересыщениях всегда сопряжено с большими ошибками. В меньшей степени от чистоты исходных веществ зависит кристаллизация при сравнительно небольших пересыщениях, при которых длительность латентных периодов выражается по крайней мере в часах. Поскольку протяженность этих периодов связана с пересыщением [5], путем экстраполяции могут быть определены значения пересыщений, при которых кристаллизации начинается мгновенно, и те, при которых она практи чески совсем не идет. [14]
ПАВ, стабилизирующие пересыщенные растворы, по характеру своего действия могут быть разделены на две группы. В присутствии добавок ПАВ первой группы ( поливиниламин, полиакрил-амид и др.) достигается устойчивое повышение стабильности пересыщенных растворов, сохраняющееся в течение длительного периода времени. Добавки ПАВ второй группы ( гексаметафосфат натрия) замедляют скорость возникновения кристаллов лишь в течение некоторого времени после переохлаждения раствора; затем действие добавок постепенно ослабевает. [15]
Страницы: 1 2