Ставерман
Cтраница 2
Точно так же Бергсма и Ставерман [19] для различных мембран и сочетаний ионов Н - Na, K - Na, H - Ag и Na - Ag измерили значения БИП и числа переноса. [16]
Более общим является приближение Гуггенгейма - Ставермана [218], позволяющее рассматривать не только линейные, но и объемные молекулы. [17]
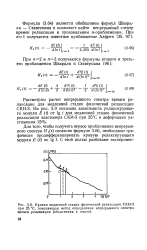 |
Кривая медленной стадии физической релаксации СКИ-3 при 25 С, поясняющая метод определения непрерывного спектра времен релаксации ( объяснения в тексте. [18] |
Формула (3.64) является обобщением формул Шварц-ля - Ставермана и позволяет найти непрерывный спектр времен релаксации в произвольном / г-приближении. [19]
Сетка стабильных узлов была рассмотрена Дьюизером и Ставерманом [146], показавшими, что в математическом отношении такая система эквивалентна ансамблю не связанных между собой цепей, отдельные точки которых характеризуются повышенным коэффициентом трения. Таким образом, хотя наличие стабильной сетки приводит к возникновению времен релаксации, намного превосходящих их максимальные значения для отдельных цепей, характер распределения времен релаксации не соответствует псевдоравновесной зоне. [20]
Проверим теоретическую зависимость (8.120) на иллюстративном примере опытов Ставермана J203 ], который изучал композит, состоящий из резины с 42 % объемным содержанием кристаллов поваренной соли. [21]
 |
Щелевой осмометр Пальса и Ставермана. [22] |
Пытаясь преодолеть трудности, связанные с несовершенством полупроницаемых мембран, Пальс и Ставерман [34] изготовили осмометр, в котором органическая пленка, используемая обычно в качестве мембраны, заменена щелью. [23]
Формулы Шмида и Гельмгольца - Смолуховского, так же как и формула Ставермана [ S98 ], приведены в табл. 2.6. Ставерман применил методы термодинамики неравновесных процессов для явления переноса в мембранах и вывел уравнения, связывающие обычные термодинамические и феноменологические постоянные, не зависящие от модели данной мембраны. Поскольку эти уравнения содержат величины, связанные с переносом как заряженных, так и незаряженных частиц, они обеспечивают связь между легко определяемыми свойствами, такими, как потенциал мембраны, электропроводность и электроосмотический перенос воды. Уравнения Ставермана имеют общий характер, они справедливы почти во всех случаях, поэтому ими можно пользоваться для проверки уравнений, выведенных из теорий Шмида и Гельмгольца - Смолуховского. [24]
При применении любого осмометра, кроме осмометра с паровой фазой Пальса и Ставермана [34], возможна диффузия растворенного вещества через мембраны. Для количественной проверки влияния диффузии растворенных молекул через мембрану осмометра на результат измерения молекулярного веса Аллен и Плейс [91] сравнивали средне-числовые молекулярные веса нескольких образцов полистирола с известным молекулярновесовым распределением. [25]
Формулы Шмида и Гельмгольца - Смолуховского, так же как и формула Ставермана [ S98 ], приведены в табл. 2.6. Ставерман применил методы термодинамики неравновесных процессов для явления переноса в мембранах и вывел уравнения, связывающие обычные термодинамические и феноменологические постоянные, не зависящие от модели данной мембраны. Поскольку эти уравнения содержат величины, связанные с переносом как заряженных, так и незаряженных частиц, они обеспечивают связь между легко определяемыми свойствами, такими, как потенциал мембраны, электропроводность и электроосмотический перенос воды. Уравнения Ставермана имеют общий характер, они справедливы почти во всех случаях, поэтому ими можно пользоваться для проверки уравнений, выведенных из теорий Шмида и Гельмгольца - Смолуховского. [26]
Метод динамического определения осмотического давления также удобен для проведения измерений вблизи нулевого времени. Однако Ставерман [37] показал, что и этот метод может приводить к ошибочным результатам. В табл. 7 приведены данные, полученные в серии опытов с мембранами, обладающими различной проницаемостью. [27]
Сравнение уравнений (2.90) и (2.28) показывает, что коэффициент Lu равен произведению подвижности и концентрации частицы i. Здесь следует указать на смысл символов, введенных Ставерманом, которые даны в табл. 2.6: Е и Р означают соответственно разность потенциалов и давлений через мембрану. [28]
Принцип ТВА в том виде, в котором был изложен выше, справедлив для материалов, относящихся к классу термореоло-гически простых. Термин термореологически простой материал был введен Шварцелем и Ставерманом [244] и относится к полимерам, для которых справедливо утверждение, что все времена запаздывания ( или релаксации) зависят от температуры одинаковым образом. Для таких материалов существует обобщенная кривая механических свойств, и коэффициент приведения является функцией только температуры. Концепции термореологически простых материалов удовлетворяют в основном эластомеры и аморфные гомополимеры. [29]
Из приведенных выше примеров следует, что используемые модели реальной структуры молекул весьма условны и способны лишь приближенно учесть молекулярную форму. Однако при расчетах комбинаторной составляющей термодинамических свойств согласно достаточно грубому приближению Ставермана более тщательное рассмотрение строения молекул вряд ли целесообразно. Описанный выше способ учета геометрии молекул аналогичен часто применяемому в решеточных моделях без вакансий. [30]
Страницы: 1 2 3