Ставерман
Cтраница 3
В описании ползучести полимеров при различных постоянных и переменных температурах важную роль играет принцип тем-пературно-временной аналогии. Материалы, удовлетворяющие принципу температурно-времен-ного соответствия, называют, следуя Шварцлю и Ставерману [244], термореологически простыми. [31]
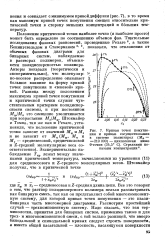 |
Кривая точек помутнения и кривые сосуществования в системе полистирол ( Мп 210 000 - циклогексан ниже 6-точки ( 34 5 С. Стрелками показаны концентрации6. [32] |
Положение критической точки наиболее точно ( и наиболее просто) может быть определено по соотношению объемов фаз. Тщательные исследования фазовых равновесий, проведенные Рехаге 6, а также Кенингсвельдом и Ставерманом 8 9, обычных фазовых диаграмм для бинарных систем, наблюдаемые в растворах полимеров, объясняются полидисперсностью полимера. Авторы показали ( теоретически и экспериментально), что молекуляр-но-весовое распределение оказывает большое влияние на форму кривой точек помутнения и теневой кривой. [33]
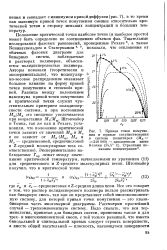 |
Кривая точек помутнения и кривые сосуществования в системе полистирол ( Мп 210 000 - циклогексан ниже 0-точки ( 34 5Ч С. Стрелками показаны концентрации6. [34] |
Положение критической точки наиболее точно ( и наиболее просто) может быть определено по соотношению объемов фаз. Тщательные исследования фазовых равновесий, проведенные Рехаге 6, а также Кенингсвельдом и Ставерманом 8 9, показали, что отклонения от обычных фазовых диаграмм для бинарных систем, наблюдаемые в растворах полимеров, объясняются полидисперсностью полимера. Авторы показали ( теоретически и экспериментально), что молекуляр-но-весовое распределение оказывает большое влияние на форму кривой точек помутнения и теневой кривой. Разница между положением максимума кривой точек помутнения и критической точки служит чувствительным критерием полидисперсности системы, и при постоянном MwjMn это смещение увеличивается при возрастании MZ / MW. Экспериментально наблюдаемые Ткр лежат между значениями критической температуры, вычисляемыми из уравнения ( 11) для средневесового и Z-среднего молекулярных весов. [35]
Параметры Л, m и п уравнения (11.70) могут быть измерены экспериментально. Однако Ставерман [36, 43] указал, что истинное осмотическое давление может быть получено, если коэффициент проницаемости а определяется методом ультрафильтрации. Несмотря на большой теоретический интерес, пока не найдено практического метода для определения молекулярных весов полимеров при использовании таких мембран. Несмотря на то что осмотические измерения, проведенные с использованием проницаемых для раствореного вещества мембран, не дают истинного значения осмотического давления, удовлетворительные результаты могут быть получены, если значение коэффициента отражения близко к единице. Правильность результатов всегда может быть проверена при использовании для определения вещества известного молекулярного веса. [36]
Формулы Шмида и Гельмгольца - Смолуховского, так же как и формула Ставермана [ S98 ], приведены в табл. 2.6. Ставерман применил методы термодинамики неравновесных процессов для явления переноса в мембранах и вывел уравнения, связывающие обычные термодинамические и феноменологические постоянные, не зависящие от модели данной мембраны. Поскольку эти уравнения содержат величины, связанные с переносом как заряженных, так и незаряженных частиц, они обеспечивают связь между легко определяемыми свойствами, такими, как потенциал мембраны, электропроводность и электроосмотический перенос воды. Уравнения Ставермана имеют общий характер, они справедливы почти во всех случаях, поэтому ими можно пользоваться для проверки уравнений, выведенных из теорий Шмида и Гельмгольца - Смолуховского. [37]
Фильтры ультрафайн хранят в 20 % - ном растворе этанола в воде; для перенесения в органический растворитель фильтры выдерживают в течение часа или более в абсолютном спирте, затем в смеси этанола с растворителем в соотношении 1: 1, после чего погружают в растворитель. Хотя свойства мембран различных партий, выпускаемых изготовителем, несколько варьируют, все же каждая партия содержит мембраны, дающие величину осмотического давления в пределах 85 - 98 % от теоретического при испытании с пентаэритритолтетрастеаратом. По данным Ставермана и Альванга, а также Сэмуельсона, осмотическое давление в этих условиях падает со временем лишь очень медленно. В табл. 8 приведены типичные результаты, полученные при исследовании растворов пентаэритритолте-трастеарата, тристеарина и октаацетата сахарозы. [38]
В зависимости от пути, который использован для достижения положения равновесия, осмометры подразделяются на газовые осмометры, мембранные осмометры и эластоосмометры. Однако на практике скорость достижения равновесия через парообразное состояние настолько мала, а теплопередача так незначительна, что этот метод не может быть использован. Несмотря на это, Пальс и Ставерман U05 ] получили удовлетворительные результаты по определению молекулярного веса полистирола вплоть до 10 000 при использовании парового щелевого осмометра, в котором мембрану заменяла щель, наполненная парами растворителя между двумя пористыми стеклянными дисками каждый толщиной 0 127 мм. [39]
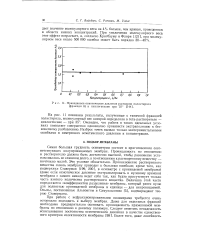 |
Приведенное осмотическое давление растворов полистирола ( фракция А в циклогексане при 35. [40] |
Самая большая трудность осмометрии состоит в приготовлении соответствующих полупроницаемых мембран. Проницаемость по отношению к растворителю должна быть достаточно высокой, чтобы равновесие устанавливалось не слишком долго, а по отношению к растворенному веществу - ничтожно малой. Проникновение растворенного вещества сквозь мембрану приводит к большим ошибкам; кроме того, как подчеркнул Ставерман [199, 200], в осмометре с проницаемой мембраной ( даже если осмотическое давление экстраполировать к нулевому времени) мембрана с самого начала ведет себя так, как будто присутствует только часть взятого количества растворенного вещества. Величина этой части определяется коэффициентом разделения мембраны, который равен нулю для полностью проницаемой мембраны и единице - для непроницаемой. Опыты, поставленные Альвонгом и Самуэльсоном [5], подтверждают теорию Ставермана. [41]
Ферри с соавторами концепция, объясняющая сдвиг длинновременной части релаксационного спектра в сторону больших времен релаксации образованием зацеплений макромолеку-лярных цепей, получила обоснование в теории А. Их модель является обобщением ранее предложенной Дж. Ставерманом модели сетки химических, связей, между узлами которой располагается вязкоупругая цепочка. Длина отрезка цепи между узлами достаточно велика, чтобы для него существовал спектр времен релаксации, описываемый моделью КСР. Особенностью модели Чомпфа - Дуйзера - Ста-вермана ( сокращенно ЧДС), является допущение возможности проскальзывания цепей в узле сетки, характеризуемое новым параметром - коэффициентом б, определяющим относительную свободу скольжения. [42]
В рамках настоящего обзора нельзя подробно рассмотреть все работы, в результате которых созданы современные представления о механизме гидролитической полимеризации капролактама. Необходимо отметить, что широкая дискуссия о механизме полимеризации капролактама вначале характеризовалась большим числом спекулятивных предположений, не имевших достаточной экспериментальной основы. В последние годы дискуссия проводится в основном между школами Германса ( Утрехт) - Ставермана ( Дельфт), с одной стороны, и Вайлота - с другой, причем основным вопросом в дискуссии в настоящее время является вопрос об удельном весе отдельных реакций в общем сложном процессе полимеризации. [43]
Самая большая трудность осмометрии состоит в приготовлении соответствующих полупроницаемых мембран. Проницаемость по отношению к растворителю должна быть достаточно высокой, чтобы равновесие устанавливалось не слишком долго, а по отношению к растворенному веществу - ничтожно малой. Проникновение растворенного вещества сквозь мембрану приводит к большим ошибкам; кроме того, как подчеркнул Ставерман [199, 200], в осмометре с проницаемой мембраной ( даже если осмотическое давление экстраполировать к нулевому времени) мембрана с самого начала ведет себя так, как будто присутствует только часть взятого количества растворенного вещества. Величина этой части определяется коэффициентом разделения мембраны, который равен нулю для полностью проницаемой мембраны и единице - для непроницаемой. Опыты, поставленные Альвонгом и Самуэльсоном [5], подтверждают теорию Ставермана. [44]
Страницы: 1 2 3