Стадия - перенос - электрон
Cтраница 1
Обратимые радикальные стадии переноса электрона и атома водорода предполагались и ранее, однако однозначные доказательства их существования были получены лишь с помощью ХПЯ. Наиболее ярко они проявляются в фотохимических реакциях, где играют важную роль в процессах деградации электронной энергии и тушения возбужденных состояний молекул. [1]
Доказательством стадии переноса электрона может служить обнаружение радикальных или ион-радикальных частиц. В связи с этим особое значение приобретает метод ЭПР, с помощью которого были получены многочисленные доказательства переноса электрона в химических реакциях ( настоящий сборник, стр. Другим методом, который позволяет изучать реакции одноэлект-ронного переноса, является метод ХПЯ. [2]
Если предположить, что стадия переноса электрона осуществляется значительно медленнее, чем стадия переноса массы, то приэлектродная концентрация электроактивных частиц равна их концентрации в массе раствора. Далее предполагается, что реакция переноса электрона состоит только из одной лимитирующей стадии, в которой переносится то же число электронов, что и в общей реакции. Рассмотрим энергетическую диаграмму, изображенную на рис. 1 - 1, где кривые А и Б - профили потенциальной энергии окисленной и восстановленной форм реакции ( 1 - 15) соответственно. Кривые потенциальной энергии соответствуют равновесному потенциалу системы, когда, согласно определению, скорости окисления и восстановления равны; АО равн - это свободная энергия активации при равновесном электродном потенциале. [3]
Поскольку электрохимические реакции включают стадию переноса электронов между электродом и окружающей его средой, некоторое внимание в главе уделено также электронной структуре объема и поверхности металлических кристаллов, а также потенциальному барьеру для эмиссии электронов в вакуум. Рассмотрена зависимость высоты этого барьера от микротопографии и ориентации кристаллов на поверхности. [4]
 |
Зависимость., от рН. [5] |
Часто протолитическая реакция протекает после стадии переноса электрона. Если собственно электрохимическая стадия необратима, то кинетика последующей протонизации не влияет на скорость электрохимического процесса в целом, а следовательно, не зависит от рН и потенциал восстановления или fi / z - Такой случай имеет место, например, при восстановлении большинства органических галогенпроизводных: на первой стадии процесса происходит обычно необратимый перенос двух электронов с образованием иона галогена и органического анион-радикала, который, присоединяя протон, образует конечный продукт восстановления. [6]
Почти для всех металлов замедленность стадии переноса электрона может быть обнаружена при использовании достаточно эффективного перемешивания раствора или с применением нестационарных методов исследования. Однако для таких металлов, как марганец, железо, никель, кобальт, замедленность стадии переноса электрона обнаруживается даже в неперемешиваемых растворах, поскольку для них характерны низкие токи обмена. Строго говоря, ток обмена является не только характеристикой металла, но и в значительной степени зависит от состава раствора. Даже в растворах простых ионов при изменении природы аниона и добавок других некомплексообразующих компонентов, например солей щелочных металлов, значение тока обмена может значительно изменяться. Как экспериментально установлено, комплексообразование обычно приводит к снижению тока обмена. [7]
Когда самая быстрая стадия является стадией переноса электрона, тогда т будет зависеть от потенциала. [8]
Гомогенные реакции, сочетающиеся со стадией переноса электрона, легко обнаруживаются по их влиянию на полярограммы. [9]
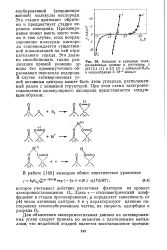 |
Анодные и катодные поляризационные кривые в растворах с рН12 1 ( / и 3 2 ( 2 с добавкой Н2О2 в концентрации 2 - 10 - 3 моль / л. [10] |
Эта стадия протекает обратимо и предшествует стадии переноса электрона. Протониро-вание может иметь место только в том случае, если координирование молекулы кислорода сопровождается существенной локализацией на ней отрицательного заряда. Это должно способствовать также реализации прямой реакции до воды без промежуточного образования пероксида водорода. В случае активированных углей активным центром может быть атом углерода, расположенный рядом с хинонной структурой. [11]
Показано, что не только сама стадия переноса электрона, но и кинетика сопряженных с ней химических реакций часто зависит от структуры двойного слоя. [12]
Получение информации о первичной стадии - стадии переноса электрона, например о стандартных потенциалах образования катион-радикалов, до последнего времени было в значительной мере затруднено из-за протекания быстрых реакций промежуточных частиц. Обратимое образование катион-радикалов обычно не удается наблюдать из-за их реакций с примесями в растворителе и ( или) быстрого отщепления протона; возникающая вследствие этого необратимость сопровождается в циклической вольтамперометрии смещением потенциала пика от потенциала обратимого окисления. [13]
В рамках предположения о почти одновременном протекании стадии переноса электрона и последней стадии диффузии расчет Эа позволяет получить скорость в виде уравнения, которое имеет такую же форму, как если бы реакция на поверхности раздела происходила в одну стадию. [14]
 |
Катодная ( / и анодная ( 2 поляризационные кривые в полулогарифмических координатах при замедленной стадии переноса электронов.| Поляризационные кривые при замедленной стадии переноса электрона. [15] |
Страницы: 1 2 3 4