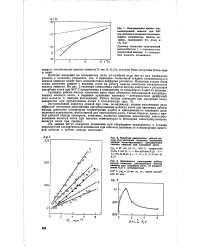
Возможная стадия
Cтраница 2
В последнем разделе обсуждаются особенности других возможных стадий электродных процессов - химических и образования новой фазы, а также многостадийные и параллельные процессы и роль явлений пассивности и адсорбции органических соединений в электрохимической кинетике. В этом разделе отражены только самые основные особенности кинетики сложных процессов и приведено ограниченное число примеров практически важных электрохимических реакций. [16]
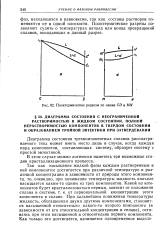 |
Политермические разрезы по линии CD и MN. [17] |
В этом случае можно логически наметить три возможные стадии кристаллизационного процесса. [18]
Образование смесей с низкой температурой плавления также было рассмотрено [8] в качестве возможной стадии в процессе растрескивания и такие смеси были идентифицированы. Однако наличие широкой области хлоридов, в которой происходит растрескивание, наводит на мысль о том, что образование таких смесей не обязательно. [19]
При этом остается нерешенным вопрос, каким образом и на какой из возможных стадий процесса совместного разряда добавка оказывает наибольший эффект. [20]
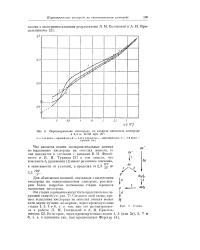 |
Перенапряжение кислорода на гладком никелевом электроде в 4 4 а. КОН при 20. [21] |
Для объяснения явлений, связанных с выделением кислорода на окисноникеловом электроде, рассмотрим более подробно возможные стадии процесса выделения кислорода. [22]
Как указывалось выше, простейшее условие (4.18) для второго предела воспламенения является приближенным, поскольку не учитывает всех возможных стадий обрыва и разветвления. Но теперь такая возможность учета всех факторов появляется. [23]
Очевидно, что для более глубокого понимания механизма действия ингибиторов необходимо знать, как влияют ингибиторы разной природы на возможные стадии катодного процесса. [24]
Величина подвижности, рассчитанная по уравнению ( 57) для вращения воды, получается значительно меньше величины, рассчитанной для любых других возможных стадий, и, следовательно, вызываемое полем вращение молекул воды в гидратных оболочках ионов Н3О при прохождении протонов через воду является стадией, определяющей скорость протонной электропроводности: собственно перенос протона в системе Н3О - Н2О может происходить с большой скоростью посредством квантовомеханического туннельного эффекта. [25]
Наличие микрофаз на поверхности ( если пб крайней мере две из них принимают участие в катализе) указывает, что, в принципе, возможной стадией каталитического синтеза аммиака может быть поверхностная диффузия реагентов. Ивановым и нами были также получены данные о влиянии азота на работу выхода электрона катализаторов синтеза аммиака. На рис. 2 величина уменьшения работы выхода электрона в результате адсорбции азота при 500 С представлена в зависимости от квадратного корня из времени. [27]
Общепринятая точка зрения состоит в том, что реакция 22 не играет важной роли в механизме сложного процесса, поскольку ее коэффициент скорости много меньше коэффициентов скорости других возможных стадий зарождения. Энергия активации прямой реакции 22 несколько выше ( - на 20 %) энергии активации обратной реакции из-за значительно большей деформации конфигурации исходных реагентов при образовании активированного комплекса. [28]
Не все из перечисленных здесь стадий возможны в конкретных системах, но обычно не составляет труда, руководствуясь перечнем Р1 - Р16 и Д1 - Д13, выявить возможные стадии в данной системе. [29]
Полученный нами на ряде металлов экспериментальный материал показывает, что кинетика выделения водорода в широкой области потенциалов не может быть описана на основании представления о замедленности только одной из возможных стадий суммарного процесса. Механизм перенапряжения на металлах, адсорбирующих водород, особенно в щелочных растворах, более сложен. Для полного описания его необходимо учитывать две, а возможно, и большее число стадий, которые в определенных областях поляризации протекают с соизмеримыми скоростями. [30]
Страницы: 1 2 3 4