Изменение - мольная доля
Cтраница 2
 |
Молекулярные взаимодействия в смешанных жидкостях.| Избыточные термодинамические функции для системы СНдОН-СС14 при 35 С. [16] |
Это видно из рис. 3.4, который показывает, что теплота смешения Д сМ метанола с четыреххло-ристым углеродом не изменяется симметрично с изменением мольных долей того и другого вещества, как этого требует уравнение (1.23), и что избыточная энтропия Д5И1б превосходит изменение энтропии при смешивании ( энтропия беспорядочного смешивания равна - NtkT In [ N1 / ( N1 N2) ] - N2kT In [ 2 / ( JV2) ]), причем это превышение существенно больше нуля. Поскольку свойства воды в значительной мере определяются водородными связями, можно заранее утверждать, что свойства водных растворов будут сильно отклоняться от свойств регулярных растворов, так что описанная выше теория окажется неприменимой. Поэтому вернемся к обширной проблеме водных растворов и рассмотрим сначала водные растворы соединений, не содержащих гидроксильных групп. [17]
Такой вклад существует у всех типов сольватокомплексов и приводит к фоновому вкладу в скорость релаксации Т) §, который монотонно изменяется с изменением мольной доли ( X) компонента В в смешанном растворителе А В. [18]
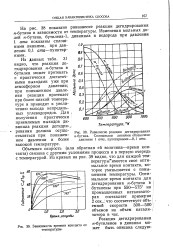 |
Равновесие реакции дегидрирования.| Зависимость времени контакта от - м-бутиленов В дивинил МО-температуры, жет быть описана следую. [19] |
На рис. 38 показано равновесие реакции дегидрирования н-бутана в зависимости от температуры. Изменения мольных долей w - бутана, бутилена-1, дивинила и водорода при давлении 1 ата показаны сплошными линиями, при дав - 1.0 лении 0 1 ста-пунктирными. [20]
При экспериментальном изучении многокомпонентных систем удобно изменять мольную долю одного из компонентов, например первого, при сохранении постоянного соотношения между мольными долями всех остальных компонентов. Такое изменение мольной доли первого компонента эквивалентно изменению числа молей этого компонента при постоянных числах молей всех остальных компонентов. [21]
Однако, как видно из рис. 66 ( кривая i), величина / (, вычисленная по этому уравнению из данных Кавасуми, не является константой. При изменении мольных долей компонентов ( например, при избытке СО2, NH3 или Н2О) она не остается постоянной. К тому же зависимость lg К от 1 / Т не прямолинейна. Таким образом, запись константы равновесия на основе суммарного уравнения процесса синтеза неверна. Выше уже отмечалось, что многие факты невозможно объяснить без учета образования карбамата аммония. Следует заметить, что относительно записи константы равновесия синтеза карбамида имеется и прямо противоположная точка зрения. Это равносильно признанию того, что равновесие ( 1) нацело смещено вправо и газовая фаза полностью отсутствует. [22]
Должно ли изменение мольной доли растворенного вещества от нуля до бесконечно малого значения всегда вызывать тоже бесконечно малые изменения в объемных и тепловых эффектах. Математика уже давно указала ( см., например, [7]), что ситуация может быть совершенно иной. [23]
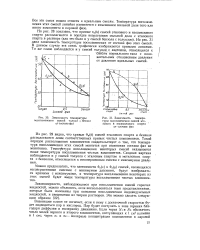 |
Зависимость температуры воспламенения смесей толуол бензол от состава фаз.| Зависимость температуры воспламенения смесей этилового и изоамилового спирта от состава фаз. [24] |
Температура воспламенения этих смесей линейно изменяется с изменением мольной доли того или иного компонента в паровой фазе. [25]
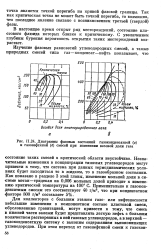 |
Диаграммы фазовых состояний газоконденсатной ( а и газонефтяной ( б смесей при изменении весовой доли газа. [26] |
Незначительные изменения в концентрации тяжелых углеводородов могут привести к тому, что система при данных термодинамических условиях будет находиться то в жидком, то в газообразном состоянии. Как показано в разделе 3 этой главы, изменение мольной доли в системе метан-тридекан на 0 006 мольных долей приводит к изменению критической температуры на 100 С. [27]
 |
Зависимости от температуры yuuipeintii резонансных. ninnii Gib ( i п СП ( 2 групп цп клопе птепа, адсорбированного на Y-АЬОз 78 ( 0 2. [28] |
В интервале температур 4 - 10 - 65 наблюдаются относительные сдвиги обеих резонансных групп ( порядка 10 - 15 Гц), которые отсутствуют при более высоких температурах. Как известно, характер зависимостей / / j: - ( Т) в этом случае определяется изменением мольной доли координированных молекул. [29]
Так как мольные доли компонентов связаны между собой уравнением (1.43), то число независимых мольных долей всегда на единицу меньше числа компонентов. Поэтому при дифференцировании по мольной доле одного из компонентов надо отчетливо указывать, за счет мольной доли какого компонента ( или за счет мольных долей каких компонентов) происходит изменение мольной доли данного компонента. Часто все дифференцирования выполняют за счет мольной доли одного только компонента, например первого. [30]
Страницы: 1 2 3