Анодная поляризационная кривая сталь
Cтраница 2
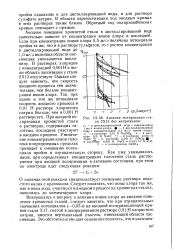 |
Анодная поляризация стали 2X13 без напряжения. [16] |
Возвращаясь к вопросу о влиянии ионов хлора на анодное поведение хромистых сталей, следует заметить, что при отрицательных значениях потенциалов ( - 0 05 в) на анодной поляризационной кривой стали Х17, снятой в деаэрированном растворе 0 01 Н хлористого натрия, имеется вертикальный участок, отвечающий области пассивации. [17]
Коррозионная стойкость стали ОХ17М1 выше, чем стали ОХ 17, но 1 % Мо не обеспечивает достаточную стойкость в концентрированной уксусной кислоте с добавками муравьиной кислоты. Анодные поляризационные кривые сталей ОХ17 и ОХ17М1 ( рис, 5) показывают, что в 90 % - ной СН3СООН в токе азота эти стали становятся пассивными примерно при одном и том же токе. Легкая поляризуемость ( большое смещение потенциала при небольшом токе) свидетельствует о торможении электродного процесса и небольшой скорости коррозии. [18]
Коррозионная стойкость стали ОХ17М1 выше, чем стали ОХ17, но 1 % Мо не обеспечивает достаточную стойкость в концентрированной уксусной кислоте с добавками муравьиной кислоты. Анодные поляризационные кривые сталей ОХ 17 и ОХ17М1 ( рис. 5) показывают, что в 90 % - ной СН3СООН в токе азота эти стали становятся пассивными примерно при одном и том же токе. Легкая поляризуемость ( большое смещение потенциала при небольшом токе) свидетельствует о торможении электродного процесса и небольшой скорости коррозии. [19]
В этом случае до рН - Ч скорость анодного процесса, в частности величина потенциала пробоя, определяется концентрацией не ионов водорода, а ионов хлора. Если в нейтральных деаэрированных средах на анодных поляризационных кривых стали 1Х18Н9Т отсутствует область активного растворения, то в средах с более низким рН сталь при тех же значениях потенциалов начинает растворяться в активном состоянии. В соответствии с изложенным в растворах азотной кислоты с рН 2 - 3 скорость коррозии стали 1Х18Н9Т практически не отличается от скорости ее в дистиллированной воде. Это объясняется тем, что с увеличением скорости катодного процесса разряда ионов водорода потенциал стали смещается в положительную сторону, что в соответствии с ходом анодной поляризационной кривой ( см. рис. 111 - 13 и 111 - 14, кривая 4) приводит к увеличению скорости коррозионного процесса. [20]
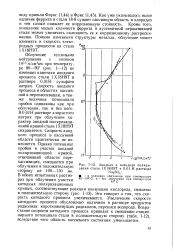 |
Анодная и катодная поляризация стали 1Х18Н9Т в 0 01 Н растворе. [21] |
Облучение тепловыми нейтронами с потоком 1012 н / см2сек при температуре 80 - 90 ( рис. 1 - 12) не изменяет кинетики анодного процесса стали 1Х18Н9Т в растворе 0 01 Н сульфата натрия. Скорость анодного процесса в областях пассивной и перепассивации, а также величина потенциала пробоя одинаковы как при облучении, так и без него. В 0 01 Н растворе хлористого натрия при облучении характер анодной поляризационной кривой стали 1X18Н97 сохраняется. Скорость анодного процесса в пассивной области практически не изменяется. Однако потенциал пробоя и участок анодной поляризационной кривой, отвечающий области перепассивации, смещаются при облучении в положительную сторону на 100 - 150 мв. [22]
В результате этого процесса сталь активируется при потенциалах более низких ( фа), чем при отсутствии галоидных ионов, при этом активирование поверхности сопровождается образованием питтингов. Адсорбция отрицательно заряженных галоидных ионов облегчается при повышении положительного электродного потенциала. Мерой стойкости стали против питтингообразования часто служит разность между потенциалом активирования и стационарным потенциалом стали ( фа-фс) [38], который для сталей, находящихся в пассивном состоянии, выше потенциала полной пассивации фп.п. Чем больше отрезок ВГ на анодной поляризационной кривой стали, тем большей устойчивостью к питтинговой коррозии она обладает. Кроме того, часто в качестве характеристики стойкости к питтинговой коррозии используют только потенциал фа, называемый в некоторых источниках потенциалом питтингообразовання или потенциалом пробоя. [23]
Страницы: 1 2