Изменение - константа
Cтраница 1
Изменение константы k при этих температурах соответствует энергии активации 4 - 5 ккал / моль. При температурах выше 35 уравнение ( 4) не соблюдается. [1]
Изменение констант в критериальных уравнениях обусловлено влиянием на тепло - и массоо бмен ботанического состава и степени разложения. [2]
Изменение константы с, являющейся мерой молекулярных сил, с концентрацией смеси может служить для отыскания образующихся в смеси химических соединений компонентов. [3]
Изменение константы k при этих температурах соответствует энергии активации 4 - 5 ккал / моль. [4]
Изменение констант и энергий диссоциации в ряду различных растворителей свидетельствует о различной степени сольватации радикала и его димера молекулами растворителя. [5]
Изменение константы определяется только отношением коэффициентов активности ионов в стекле. [6]
Изменения констант передачи и обрыва цепи в зависимости от природы комплекса при действии комплексами трехфтористого бора несколько меньше, чем в случае упомянутых катализаторов Фриделя - Крафтса, но тоже достаточно резки. [7]
Изменение константы фракционирования при добавлении ионов, имеющих знак заряда, одинаковый со знаком заряда захватываемого иона, особенно в случае присутствия в растворе многозарядных ионов того же знака. [8]
Изменение константы Бренстеда Ккисл. [9]
Изменение константы экранирования обусловлено образованием химической связи с лигандами и проявляется в изменении энергии К - или L-края поглощения. Это изменение мало по сравнению с энергией / ( ( /) - края ( - 0 1 - 0 01 %), но вполне достаточно для изучения химической связи. [10]
Изменение константы ячейки с температурой учитывалось расчетно. [11]
Изменение констант кислотности при возбуждении может достигать нескольких порядков, причем при возбуждении в синглетные состояния изменения, как правило, гораздо значительнее, чем при возбуждении в триплетные состояния. Если изменение констант кислотности достаточно велико, за время жизни возбужденного состояния может произойти присоединение или отщепление протона. [12]
Изменения константы СТС протонов обычно не очень велики, но изменения констант СТС азота и 13С могут быть вполне заметны. [13]
Изменение константы фазового равновесия одного из компонентов при добавлении растворителя или экстр-агента наблюдается для неидеальных растворов, которые не подчиняются закону Рауля. При этом степень отклонения от закона Рауля должна быть различной для растворов разделяемых компонентов. Степень отклонения от закона Рауля определяется полярностью растворяемого компонента. [14]
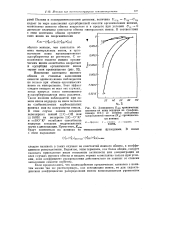 |
Зависимость Я0бм органических катионов на ионы водорода на сульфока-тионите КУ-1 от степени заполнения адсорбционной емкости ( NR органическими ионами. [15] |
Страницы: 1 2 3 4