Изменение - константа - скорость
Cтраница 1
Изменение констант скорости и константы равновесия в зависимости от температуры в хлорнокислом растворе, по данным Рабидо и Клайна [37], изображено на рис. 2.8. Энергия активации для прямой реакции равна 14 2 ккал / моль и для обратной реакции 5 42 ккал / моль. [1]
Изменение константы скорости разложения для одной и той же амальгамы при переходе от одного деполяризатора к другому, в отсутствие с уравнением [4.55], должно зависеть от величин потенциалов электрохимического восстановления этих соединений. [2]
Изменение констант скорости поликоординации с температурой протекает в согласии с уравнением Аррениуса. Энергия активации поликоординации п - бмс - ( ацетоацетил) дифенилоксида с ацетилацетонатом бериллия в среде диметилформамида составляет 25 ккал / молъ. [3]
Изменение константы скорости превращения 2 3 4-триметилпентана в концентрированной серной кислоте. [4]
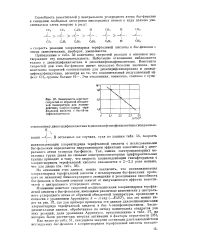 |
Зависимость констант скоростей от обратной абсолютной температуры для взаимодействия хлорангидрида терефталевой кислоты с бие - ( 4-ок-сифенил метаном. [5] |
Изменение констант скоростей поликонденсации хлорангидрида терефталевой кислоты с быс-фенолами, имеющими различные заместители у центрального углеродного атома от обратной абсолютной температуры, происходит в согласии с уравнением Аррениуса: k - А ехр ( - E / RT), как это можно ви-дет на рис. 37, где для примера приведены эти данные для поликонденсации хлорангидрида терефталевой кислоты в бис - 4-оксифенил) метаном. Экспериментальные данные, обработанные по методу наименьших квадратов для этих реакций, дали уравнения Аррениуса. [6]
Такое огромное изменение константы скорости для очень небольшого ( и легко достижимого) изменения условий показывает, насколько важны электрохимические методы контроля за скоростями реакций. Частичное объяснение причины такого большого изменения можио получить, выразив разность потенциалов через электрическое поле, действующее на ион в двойном слое. Разность потенциалов 1 В в двойном слое толщиной 10 - 9 м ( несколько молекулярных диаметров) соответствует электрическому полю 109 В / м, или 30 МВ / см. Едва ли вызывает удивление. Электрохимия с внешней стороны кажется слабосильной, но более глубокое исследование процессов, происходящих на молекулярном уровне, показывает, насколько велик электрический стресс при переходе электронов от иопов к электроду или при отрыве ионов от электрода. [7]
Такое огромное изменение константы скорости для очень небольшого ( и легко достижимого) изменения условий показывает, насколько важны электрохимические методы контроля за скоростями реакций. Частичное объяснение причины такого большого изменения можно получить, выразив разность потенциалов через электрическое поле, действующее на ион в двойном слое. Разность потенциалов 1 В в двойном слое толщиной 10 - 9 м ( несколько молекулярных диаметров) соответствует электрическому полю 109 В / м, или 10 МВ / см. Едва ли вызывает удивление, что при таком изменении электрического поля происходят огромные изменения констант скоростей. Электрохимия с внешней стороны кажется слабосильной, но более глубокое исследование процессов, происходящих на молекулярном уровне, показывает, насколько велик электрический стресс при переходеэлектропов от иоцов к электроду или при отрыве ионов от электрода. [8]
Такое огромное изменение константы скорости для очень неболь шого ( и легко достижимого) изменения условий показывает, на сколько важны электрохимические методы контроля за скоростя ми реакций. Частичное объяснение причины такого большого из менения можно получить, выразив разность потенциалов чере; электрическое поле, действующее на ион в двойном слое. Раз ность потенциалов 1 В в двойном слое толщиной 10 - 9 ( несколько молекулярных диаметров) соответствует электриче скому полю 109 В / м, или 10 МВ / см. Едва ли вызывает удивление что при таком изменении электрического поля происходят огром ные изменения констант скоростей. Электрохимия с внешней сто роны кажется слабосильной, но более глубокое исследованш процессов, происходящих на молекулярном уровне, показывает насколько велик электрический стресс при переходеэлектропов oi иоцов к электроду или при отрыве ионов от электрода. [9]
Сопоставим изменение констант скоростей процесса релаксации двух резин на основе СКН-18 наирит Б и СКН-40 при действии на них масел - полиэфирного Б - ЗВ и полисилоксано-вого ПЭС-С-1. В масле ПЭС-С-1 масса обеих резин уменьшается, что связано с вымыванием части составляющих резину ингредиентов и соответствующим уменьшением размеров образца. На рис. 62 представлена температурная зависимость логарифмов констант скоростей химической релаксации, рассчитанных из кинетических кривых накопления остаточной деформации и релаксации напряжения при старении указанных резин в соответствующих маслах. [10]
Сопоставим изменение констант скоростей процесса релаксации двух резин на основе СКН-18 - f - наирит Б и СКН-40 при действии на них масел - полиэфирного Б - ЗВ и полисилоксано-вого ПЭС-С-1. В масле ПЭС-С-1 масса обеих резин уменьшается, что связано с вымыванием части составляющих резину ингредиентов и соответствующим уменьшением размеров образца. На рис. 62 представлена температурная зависимость логарифмов констант скоростей химической релаксации, рассчитанных из кинетических кривых накопления остаточной деформации и релаксации напряжения при старении указанных резин в соответствующих маслах. [11]
Характер изменения константы скорости при переходе от одного периода к другому устанавливают на основании статистических данных. [12]
Отсутствие изменения константы скорости указывает на гомогенный характер реакции. [13]
 |
Константы скорости термического разложения азодинптрилов в среде толуола при 80 2 С.| Константы скорости разложения 2 2 -азо-б с -. 13обутиронитрила в различных растворителях при 80 2 С. [14] |
Причина изменения констант скоростей, связанных с влиянием величины радикала R, делается понятной, если сравнить взаимное пространственное влияние групп, находящихся на обоих концах молекулы, при переходе от метила к нормальному бутилу. Влияние радикала, если R-изобутильная группа, оказывается очень сильным, поскольку в этом случае из-за пространственных затруднений свобода колебательных движений радикалов, находящихся у связи - NN -, в значительной степени снижается. Напротив, взаимное пространственное влияние циклогек-сильных групп 1 1 -азо-бмс - ( 1-циклогексилцианида) невелико. [15]
Страницы: 1 2 3 4