Изменение - константа - скорость
Cтраница 2
Учет изменения констант скорости приводит к выводу о незначительном торможении реакции давлением. [16]
Характер изменения константы скорости при переходе от одного периода к другому устанавливают на основании статистических данных. [17]
Зависимости изменения константы скорости образования комплекса и продолжительности выжига половины отложенного кокса имеют одинаковый характер. Это показывает, что влияние металлов на выжиг коксовых отложений заключается в ускорении первой стадии процесса - образования углеродно-кислородного комплекса вследствие их способности катализировать реакции окисления. [18]
При изменении константы скорости сушки могут быть рассчитаны значения переходного влагосодержания. [19]
Определено [185] изменение константы скорости крекинга от добавления в сырье азотистых оснований. Как видно из табл. 40, при добавке 0 1 вес. Константы скорости крекинга газойля ( & о) и образования бензина ( k) уменьшаются при этом почти вдвое. На селективность крекинга хинолин почти не влияет. [20]
До наступления изменения константы скорости роста цепи средняя молекулярная масса полимера практически не зависит от времени полимеризации. Однако при наличии в реакционной среде примесей, способных реагировать с макрорадикалами, степень полимеризации вначале - будет иметь пониженное значение, а после израсходования примесей приобретает нормальную величину. [21]
Таким образом, изменение константы скорости по ходу температурной кривой отражает влияние на кинетику процесса не только температуры, но и изменения состава реакционной смеси. [22]
В этом случае изменение константы скорости электрохимической реакции, как и константы скорости химической реакции, определяется, вероятно, также уравнениями Хаммета - Тафта. [23]
В этом случае изменение константы скорости электрохимической реакции, как и константы скорости химической реакции, определяется, по-видимому, также уравнениями Гаммета - Тафта. [24]
Ввиду огромного диапазона изменения константы скорости, нужно было бы предположить неправдоподобные погрешности ( порядка 8 ккал в величине Е) при определении активационных параметров, чтобы наблюдаемое явление могло быть объяснено за счет экспериментальных ошибок. [25]
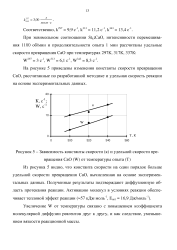 |
Зависимость константы скорости ( к и удельной скорости превращения СаО ( W от температуры опыта ( Т. [26] |
На рисунке 5 приведены изменения константы скорости превращения СаО, рассчитанные по разработанной методике и удельная скорость реакции на основе экспериментальных данных. [27]
 |
Диаграмма потенциальной энергии для реакции Н2 I2 2HI. [28] |
Изменение температуры всегда вызывает изменение константы скорости химической реакции. Однако некоторые превращения, например радиоактивный распад атомов, подчиняющиеся уравнению реакции первого порядка, не зависят от изменений температуры, которые могут быть созданы в лабораторных условиях. Очевидно, в этом случае изменения величины Ink слишком малы, чтобы можно было заметить влияние температуры на константу скорости радиоактивного распада. Следовательно, уравнение (13.8) практически неприменимо к радиоактивному распаду. [29]
На рис. 46 показано изменение константы скорости магний-хромового катализатора с добавкой кремневой кислоты, процент которой отложен по оси ординат. Если при добавлении промотора Е и k0 сначала снижаются, а затем растут, то при низких температурах должен быть максимум, при высоких - минимум. На рис. 47 показано изменение активности закиси никеля при введении нитрата бария, подтверждающее сказанное выше. Относительно большое количество промотирующей добавки может привести к отравлению катализатора - потере им каталитической активности. [30]
Страницы: 1 2 3 4