Изменение - электронная конфигурация
Cтраница 1
 |
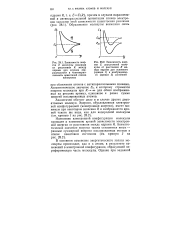
Диссоциация кислорода гемоглобина Н и нормального гемоглобина. [1] |
Изменения электронной конфигурации d - орбиталей железа определяются связыванием лиганда как в ферро -, так и в ферри-производных гемоглобина и миоглобина. [2]
Изменение электронной конфигурации, а следовательно, увеличение сопряжения связей в анионах и образование группы НбОа определяют изменение энтальпии и энтропии в процессе диссоциации. [3]
Изменение электронной конфигурации молекулы приводит к изменению кривой зависимости электронной энергии от расстояния между ядрами R. [5]
Однако изменение электронной конфигурации катиона при реакции не является необходимым условием каталитической активности и реакция Н2 с D2 может протекать на таких окислах, как MgO и А1203, катион которых не изменяет своего валентного состояния. [6]
При изменении электронной конфигурации на один электрон ( d6), например в Сош, довольно резко изменяются свойства комплексов. Все комплексы Со 1 октаэдрические и почти все низкоспиновые, чему способствуют значения энергии спин-спаривания и энергии СКП, особенно при сильном поле лигандов. Энергия СОО для низкоспиновых комплексов уменьшается вдвое; кроме того, меньший заряд иона не благоприятствует созданию сильных полей и спин-спариванию. Следовательно, большинство комплексов Со будут высокоспиновыми октаэдрическими комплексами со склонностью к окислению, особенно если лиганды создают сильное поле. [7]
Чем объясняется непоследовательное изменение электронных конфигураций в ряду актинидов. [8]
Координация сопряжена с изменением электронной конфигурации лигандов и в результате приводит к изменению их свойств. Это хорошо видно на примере кислотно-основных свойств комплексных соединений. [9]
Еще более чувствительной характеристикой изменений электронной конфигурации молекул служат величины интенсивностей полос поглощения. [10]
Поглощение света приводит к изменению электронной конфигурации, переходу молекулы в возбужденное состояние. Так как МО квантованы по энергии, это же справедливо и для полной энергии молекулы, а значит, и для разностей энергий различных ее состояний. В соответствии с этим электронно-возбужденное состояние молекулы отделено от основного состояния энергетическим интервалом указанного выше порядка. [11]
Регибридизационные дефекты связаны с возможностью изменения электронной конфигурации атомов. [12]
 |
Строение тема и его связь с белком в цитохромер450. [13] |
При связывании субстрата с цитохромом р450 происходит изменение электронной конфигурации атома железа. Связывание субстрата 1-ого типа с белковой частью цитохрома р450 железо, которое находилось в свободном ферменте в низкоспиновом состоянии, переходит в высокоспиновое состояние, происходят спектральные изменения при 390 нм. [14]
Вопрос об интенсивностях ИК-полос настолько тесно связан с изменениями электронной конфигурации в процессе колебания, что в явном виде может быть решен только путем расчета полной волновой функции молекулы. Было сформулировано математическое описание этого явления, представляющее некоторую ценность при расчете моментов связей, но априорный расчет интенсивностей полос поглощения столь груб, что почти не имеет практического значения. Однако эмпирические корреляции интенсивности со структурой иногда полезны. [15]
Страницы: 1 2 3