Изменение - электронная конфигурация
Cтраница 2
Прежде всего обращает на себя внимание периодичность в изменении электронных конфигураций атомов элементов в зависимости от порядкового номера. Это указывает, что в основе систематики химических элементов лежит электронное строение атомов. В связи с этим номер периода совпадает с главным квантовым числом внешних электронов атома. Исключение составляет первый период, содержащий только водород и гелий. [16]
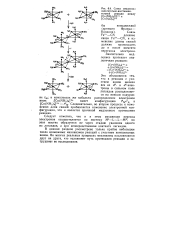 |
Схема механизма окислительно-восстановительной реакции между [ Со ( МН3 5С1 ] 2 и [ Сг ( Н20 6р. [17] |
Следовательно, во втором процессе к изменению длин связей прибавляется изменение электронной конфигурации, что и является причиной медленного протекания реакции. [18]
Согласно принципу Франка - Кондона, в процессе возбуждения происходит изменение только электронной конфигурации растворенной молекулы и окружающих ее молекул растворителя без изменения конфигурации ядер. Конечное возбужденное состояние при этом называют франк-кондоновским возбужденным состоянием. [19]
Взаимодействие сульфофталеинов с рядом катионов в кислой области, сопровождающееся изменением электронной конфигурации системы, может свидетельствовать об участии атома кислорода недиссоциированного фенольного гидроксила в координации катионов. Это согласуется с результатами исследования других комплек-сонов, содержащих фенольный гидроксил. [20]
Согласно этому принципу, в процессе электронного возбуждения молекулы в растворе происходит изменение только электронной конфигурации растворенной частицы и бли-кайших молекул растворителя без изменения конфигурации ядер. [21]
Цвет молекулы красителя зависит от многих особенностей ее строения и является результатом изменения электронной конфигурации. [22]
Поглощение электромагнитного излучения одноатомными газами, например парами натрия, приводит к высокоспецифичному изменению электронной конфигурации. [23]
Таким образом, низкая активность Сг203 вызвана превращением в re - полупроводник и изменением электронной конфигурации катиона d3 в d, т.е. превращением катиона в структуру непереходного металла. [24]
В группах веществ-аналогов, как давно было замечено, свойства меняются определенным образом, отражающим изменение электронных конфигураций при постепенном изменении химического состава, например, при переходе одной из составляющих соединения вниз по периодической системе в пределах одной подгруппы. Правильно, закономерно меняются свойства и при переходе от одного вещества к другому и в изоэлектронных рядах. Это важное наблюдение используется обычно и при выборе веществ и при прогнозах их свойств. Однако мысль о связи полупроводниковых свойств веществ с их химической природой, оттолкнувшись от серого олова, о котором говорилось выше, с большим трудом пробивала себе дорогу и только в настоящее время кажется бесспорной. [25]
При этом cf - электроны могут заметно влиять на те свойства, которые связаны с изменением электронной конфигурации при переходе от чистых элементов к интерметаллическим соединениям. [26]
В предыдущем разделе мы видели, что изменение реакционной способности элементов третьего периода основано на изменении электронных конфигураций атомов. Элементы, имеющие высокую энергию ионизации и свободные валентные орбиты, обычно присоединяют электроны и действуют как окислители. Элементы, у которых энергия ионизации заметно ниже, имеют тенденцию отдавать электроны и действуют как восстановители. [27]
Примесные ядра, находясь в чужой матрице, локально возбуждают ее, но и в самом примесном атоме происходят изменения электронной конфигурации вследствие взаимодействия примеси с атомами основной решетки. Это изменение, а именно изменение распределения электронов вокруг примеси, определяется потенциальными полями кристаллической решетки. Следовательно, величина изомерного сдвига на примесном ядре в разных матрицах должна характеризовать электронное строение матрицы. [28]
Другим серьезным недостатком этой теории является то, что, рассматривая электронную конфигурацию только комплексообразователя, она не учитывает изменения электронной конфигурации лигандов. Отметим прежде всего возможность образования связей более высокого порядка - двойных или тройных, обозначаемых обычно как л-связи. Так как возникновение последних в большой степени зависит от конкретной электронной структуры лиганда, то их существование не может быть описано в рамках теории кристаллического поля. [29]
 |
Спектр поглощения паров более коротковолновых полос, хлористого водорода в близкой инфра - являющихся вибрационно-рота-красной области ционными. Теория эта хорошо. [30] |
Страницы: 1 2 3