Изменение - концентрация - катализатор
Cтраница 2
При первом способе регулируют тепловыделение в реакционной зоне изменением соотношения потоков реагирующих ве-деств, изменением концентрации катализатора и активатора. [16]
Вводя в опыт новую переменную - температуру реакции - и рассматривая процесс образования оксикарбоновых кислот при изменении концентрации катализатора, замечаем, что этот процесс развивается строго по одному и тому же закону. [17]
Молекулярная масса полиизопрена практически не зависит от конверсии, возрастает с понижением температуры полимеризации и при повышении концентрации мономера, мало изменяется с изменением концентрации катализатора ( рис. 7) [42], В определенных условиях [63] в полимеризационной системе практически сразу устанавливается стационарное ММР, характеризующееся симметрией, малой относительной дисперсией и максимумом в высокомолекулярной области. [18]
Так, например, дальнейшее прибавление катализатора вызывало в одних случаях повышение скорости полимеризации, в других - ее понижение, в то время как в иных случаях изменение концентрации катализатора практически не оказывало никакого влияния. Во всяком случае есть основания предполагать, что причина этих противоречий кроется в различной степени высушивания используемых реагентов. Поэтому особого внимания заслуживают опыты, которые были проведены с совершенно безводными реагентами при тщательном исключении влажности и добавлении строго определенных количеств воды. [19]
В каталитических реакциях, особенно гомогенных, в состав активного комплекса иногда входит одно из исходных веществ или один из продуктов реакции и, таким образом, в ходе реакции происходит изменение концентрации катализатора. [20]
В каталитических реакциях, особенно гомогенных, в состав активного комплекса иногда входит одно из исходных веществ или один из продуктов реакции, и, таким образом, в ходе реакции происходит изменение концентрации катализатора. Такие процессы получили название вток а1ШШ1 шески. [21]
Степень превращения исходных реагентов зависит от концентрации катализатора, поэтому можно изменять ее так, чтобы в начале реакционного элемента концентрация катализатора была минимальной, а к концу его возрастала до возможного максимума. Естественно, что характер изменения концентрации катализатора должен находиться в соответствии с законом выделения тепла и уравнениями кинетики. [22]
Как видно из рисунка, начиная с определенных значений концентрации катализаторов, скорость окисления достигает предельной постоянной величины. Постоянство скорости сохраняется при изменении концентрации катализатора приблизительно в 10 раз. [23]
Предполагают, что катализаторы влияют только на скорость реакции. Однако в некоторых случаях при обратимой гомогенной реакции ( реакция этерификации) равновесные концентрации компонентов, вероятно, изменяются с изменением концентрации катализатора. Так, Тримбль и Ричардсон51 установили, что кажущаяся константа равновесия реакции между этиловым спиртом и уксусной кислотой при 30 С возрастает в 4 раза при увеличении концентрации хлорной кислоты от нуля до 25 мол. Джонс и Лапорт52, ранее отметившие каталитическое влияние соляной кислоты на эту реакцию, предположили, что оно может быть вызвано гидратацией соляной кислоты, в результате которой изменяется активная концентрация или степень ассоциации молекул воды. Безусловно, аналогичное объяснение может быть справедливо и для кажущегося сдвига равновесия, замеченного в присутствии хлорной кислоты. [24]
Учет кинетических факторов позволяет наметить метод интенсификации процесса путем уменьшения температурного пика ( см. рис. 41, стр. Так, например, рассредоточение катализатора по трубке в соответствии с кинетическим законом реакции ( загрузка слоями различной длины вперемежку со слоями инертного материала или разбавление катализатора инертным материалом для изменения концентрации катализатора по длине трубки), а также увеличение скорости газов, улучшающее условия теплообмена, способствуют уменьшению температурного пика. [25]
Кинетический контроль суммарного процесса может определяться скоростями реакций ( I) или ( II), но может осуществляться и смешанный контроль. Один из способов определения времен жизни анион-радикала А базируется на переходе системы А - - Р or кинетического контроля одной из реакций ( I) или ( II) к смешанному контролю при изменении концентрации катализатора. [26]
Применяя в качестве катализатороь стеараты алюминая, кобальта, бария, церия, никеля, кадмия, цинка, окись ртути, перекись бария, перекись марганца, пермакганат калия -, свежеприготовленную водную перекись марганца, стеариновую кислоту и другие жирные кислоты, он делает заключение, что все эти катализаторы по своей эффективности мало отличаются друг от друга. Изменение концентрации катализатора мало сказывается на его эффективности Например, увеличение концентрации стеарата Mr. I до 5 % не повышает скорости процесса. [27]
Более эффективным является гомогенный катализатор, представляющий собой марганец-натриевые или марганец-калиевые соли синтетических жирных кислот. В качестве сырья для получения компонентов катализатора используют 25 % - ный раствор сульфата марганца, 40 % - ный раствор гидроксида натрия и фракцию синтетических жирных кислот GS-Сю. С изменением концентрации катализатора в реакционной смеси выход кислот меняется. На скорость процесса жидкофазного окисления парафина большое влияние оказывает температура. Поэтому во избежание повышения температуры процесса выделяемое тепло необходимо отводить. [28]
При пересчете уравнений (III.49) - (III.53) в соответствии с поставленной задачей управления оказались незначимы коэффициенты при переменных С1, , С. Это хорошо согласуется с технологическим процессом ( см. гл. I), так как изменение концентрации катализатора, подаваемого во II, III и V секции колонны, влияет на вязкость значительно меньше, чем изменение концентрации катализатора в I секции. [29]
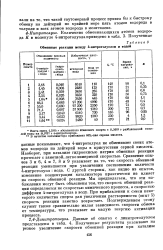 |
Обменные реакции между 4-нитротолуолом и водов. [30] |
Страницы: 1 2 3