Изменение - концентрация - азотная кислота
Cтраница 1
Изменение концентрации азотной кислоты, поступающей на концентрирование, в пределах 0 5 - 1 % не имеет существенного значения. Такие колебания очень редки и носят суточный или даже сезонный характер. [1]
Изменение концентрации азотной кислоты от 0 25 до 8 М дает возможность судить о роли ее при экстрагировании урана. [2]
Поэтому изменение концентрации азотной кислоты, изменяющее ее окислительные свойства, также изменяет скорость растворения никеля. [3]
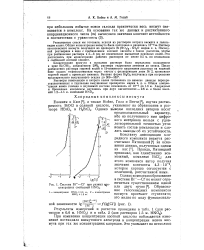 |
Система Bi - С1 при разных центрациях свободной HNO3. [4] |
При изменении концентрации азотной кислоты наблюдается изменение потенциала висмутового электрода и концентрации ионов висмута при тех же концентрациях хлоридов. [5]
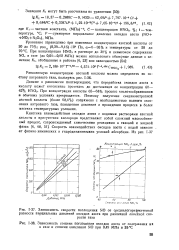 |
Зависимость степени поглощения оксидов азота от содержания их в газе и степени окисления NO при 0 49 МПа и 35 С. [6] |
Уравнение справедливо при изменении концентрации азотной кислоты от 30 до 70 %; PNOX ( 0 39 - 9 16) - 1 04 Па, а6 - 95 % и температуры от 20 до 70 С. [7]
Вильяме и Уинклер [54], изучив влияние изменения концентрации азотной кислоты и нитрата аммония на выход гексогена при получении его из уротропина, мононитрата уротропина и динитрата уротропина ( при 35 С), определили, что энергия активации для этих исходных соединений составляет соответственно И, 12 и 16 5 ккал. В то время как между двумя первыми показателями нет заметной разницы, показатель для динитрата уротропина значительно выше. На этом основании авторы утверждают, что динитрат уротропина не является промежуточным соединением при нитролизе уротропина в присутствии нитрата аммония и уксусного ангидрида. [8]
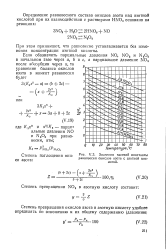 |
Значения частной константы равновесия окислов азота с азотной кислотой. [9] |
При этом принимают, что равновесие устанавливается без изменения концентрации азотной кислоты. [10]
За исключением небольшой части изотерм растворимости, где наблюдается переход гексагидрата нитрата магния в дигидрат, во всем диапазоне изменения концентрации азотной кислоты и для всех температур растворимость нитрата магния уменьшается с увеличением концентрации азотной кислоты. В 100 % - ной азотной кислоте нитрат магния практически нерастворим. [11]
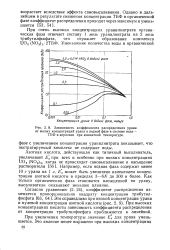 |
Зависимость коэффициента распределения урана. [12] |
Например, если водная фаза содержит менее 10 г урана на 1 л, Е а может быть увеличено изменением концентрации азотной кислоты в пределах 3 - 6jV до 300 и более. Как только органическая фаза становится насыщенной по урану, высаливатели оказывают меньшее влияние. [13]
Коэффициент распределения зависит от концентрации азотной кислоты в водной фазе и поэтому уран может быть либо экстрагирован, либо вновь возвращен в водную фазу при изменении концентрации азотной кислоты. Такие процессы включают как химическую реакцию, так и стадии подвода и отвода веществ. В целом скорость процесса зависит от скорости составляющих стадий. Для экстракции урана и большинства аналогичных процессов скорость химической реакции сравнительно выше скорости массопередачи между двумя фазами и поэтому справедливо пренебречь реакцией и рассматривать процесс, как простую массопередачу. [14]
Сравнение схем ( 1), ( 2) и ( 3) показывает, что только скорость реакции нитрования ( 1) находится в прямой зависимости от концентрации азотной кислоты, что подтверждается экспериментально; эта зависимость не одинакова для о - и п-нитрофенолов, поэтому отношение орто: пара варьирует с изменением концентрации азотной кислоты. Реакция образования нитрофенолов из нитрозофенолов ( 2) не находится в дря-мой зависимости от концентрации азотной кислоты; в количественном отношении выход нитрофенолов по этой реакции, однако, значительно меньше, чем по реакции ( 1), вследствие чего указанная зависимость отношения орто: пара от концентрации азотной кислоты не подвергается значительным изменениям. [15]
Страницы: 1 2