Изменение - концентрация - последнее
Cтраница 1
Изменение концентрации последних позволяет регулировать цветность [ ДЛ. [1]
 |
Проточная система для определения глюкозы. [2] |
Поскольку Н2О2 реагирует с иодидом в стехиометрических соотношениях, изменения концентрации последнего могут быть измерены с помощью 1 - - селек-тивного электрода. Два 1 - - се-лективных электрода ( индикаторный и электрод сравнения) разделяли замедляющим змеевиком, и камеру, в которой происходила реакция, помещали в поток раствора. [3]
Часто наблюдалось, что спектр водорастворимого красителя, введенного в раствор ПАВ, изменяется с изменением концентрации последнего. На этом явлении основан один из методов определения ККМ. [4]
 |
Влияние концентрации гидроксилами-на на константу скорости реакции псевдопервого порядка при взаимодействии его с 3 - 10 - 4Л4 аниона пировиноградной кислоты в 0 1 М фосфатном буфере. [5] |
На рис. 2 показано изменение порядка реакции между анионом пировиноградной кислоты и гидроксиламином, наблюдающееся при изменении концентрации последнего. При низких концентрациях гидроксиламина только небольшая часть аниона пировиноградной кислоты превращается в продукт присоединения, и скорость реакции пропорциональна концентрации гидроксиламина. По мере увеличения концентрации гидроксиламина все большая часть аниона пировиноградной кислоты превращается в продукт присоединения, и при высокой концентрации гидроксиламина скорость реакции не зависит от его концентрации, так как этот анион полностью превратился в продукт присоединения. [6]
 |
Распределение температур по радиусу цилиндра при граничных условиях 3-го рода 1 - экспериментальные данные. 2 - расчетные. [7] |
Такие зависимости были получены в соответствии с даннтлми М. И. Темкина и Н. В. Кульковой [10] по кинетике процесса окисления этилена, в интервале изменения концентраций последнего от 3 11 до 2 8 %, когда можно по предварительным расчетам ожидать примерно постоянной температуры по оси трубки ( dt / dx 0) и наиболее интенсивного выделения тепла на единицу объема. [8]
 |
Распределение температур по радиусу цилиндра при граничных условиях 3-го рода 1 - экспериментальные данные. 2 - расчетные. [9] |
Такие зависимости были получены в соответствии с данными М. И. Темкина и Н. В. Кульковой [10] по кинетике процесса окисления этилена, в интервале изменения концентраций последнего от 3 11 до 2 8 %, когда можно по предварительным расчетам ожидать примерно постоянной температуры по оси трубки ( dt / dx 0) и наиболее интенсивного выделения тепла на единицу объема. [10]
Как экспериментально показано в работе [100] 1, в качестве чувствительного параметра на изменение частоты обмена между радикалом и парамагнитным центром иной природы ( при изменении концентрации последнего) может служить интенсивность компонент спектра ЭПР радикала, аналогично тому, как это уже отмечалось выше при разборе работы [96] и диполь-дипольного взаимодействия между центрами. [11]
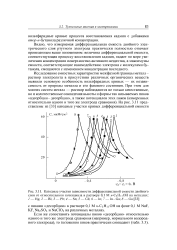 |
Катодные участки зависимости дифференциальной емкости двойного слоя от относительного потенциала в растворе 0 1 М н - CsHnOH на металлах. [12] |
Видно, что измеряемая дифференциальная емкость двойного электрического слоя ртутного электрода практически полностью отвечает приведенным выше положениям: величина дифференциальной емкости, соответствующая процессу восстановления кадмия, падает по мере увеличения концентрации поверхностно-активного вещества, а максимумы емкости, соответствующие взаимодействию электрона с молекулами бу-танола, смещаются с изменением концентрации последнего. [13]
 |
Измерение ЭДС электродной системы рН - метра.| Влияние температуры раствора на ЭДС электродной. [14] |
Он отражает свойство преломления второй среды по отношению к первой. Если преломление луча происходит в растворе, то при изменении концентрации последнего будет изменяться и показатель преломления. [15]
Страницы: 1 2