Изменение - концентрация - реагирующее вещество
Cтраница 3
В каскаде реакторов изменение концентрации реагирующих веществ носит ступенчатый характер, так как продукт реакции предыдущего реактора ( или секции) является исходным реагирующим веществом в последующем реакторе. Гидродинамический режим работы каскада реакторов является промежуточным и зависит от числа аппаратов, с увеличением числа которых он приближается к режиму полного вытеснения. В каскаде увеличивается время пребывания реагирующих компонентов по сравнению с реактором полного перемешивания, а также возрастает выход целевого компонента. [32]
 |
Реакторы смешения. [33] |
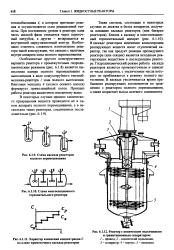
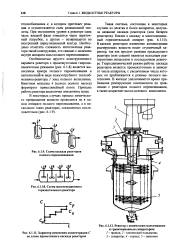
В каскаде реакторов изменение концентрации реагирующих веществ носит ступенчатый характер ( рис. 6.5 в), так как продукт реакции предыдущего аппарата является исходным реагирующим веществом в последующем аппарате. [34]
В каскаде реакторов изменение концентрации реагирующих веществ носит ступенчатый характер, так как продукт реакции предыдущего реактора ( или секции) является исходным реагирующим веществом в последующем реакторе. Гидродинамический режим работы каскада реакторов является промежуточным и зависит от числа аппаратов, с увеличением числа которых он приближается к режиму полного вытеснения. В каскаде увеличивается время пребывания реагирующих компонентов по сравнению с реактором полного перемешивания, а также возрастает выход целевого компонента. [36]
Скорость реакции определяется изменением концентрации реагирующих веществ в единицу времени. [37]
Причем наряду с изменением концентрации реагирующих веществ или функциональных групп нужно рассматривать изменение ММР макромолекул и других топологических характеристик системы. [38]
Скорость реакции измеряется изменением концентрации реагирующих веществ в единицу времени. В химической кинетике обычно пользуются молярными концентрациями, показывающими, сколько грамм-молекул ( молей) вещества содержится в одном литре. [39]
Под скоростью реакции понимается изменение концентрации реагирующих веществ в единицу времени. Чтобы вычислить скорость реакции, необходимо знать, насколько изменилась концентрация одного из реагирующих веществ в единицу времени. [40]
Под скоростью реакции понимается изменение концентрации реагирующих веществ в единицу времени при постоянном объеме. При этом концентрацию обычно выражают числом молей вещества на единицу объема реакционной смеси ( обычно на 1л), время - в секундах. Чтобы вычислить скорость реакции, необходимо знать, на сколько изменилась концентрация одного из реагирующих веществ в единицу времени. [41]
Скорость реакции зависит от изменения концентрации реагирующих веществ в единицу времени. Поскольку скорость реакции изменяется во времени, то различают среднюю и истинную скорость реакции. [42]
Концентрационная поляризация возникает вследствие изменения концентрации реагирующих веществ из-за замедленности массопереноса. [43]
Скорость реакции представляет собой изменение концентраций реагирующих веществ в единицу времени и является величиной весьма непостоянной даже при одинаковых температурах, так как концентрация исходных веществ уменьшается, а конечных - увеличивается. Тем более непостоянна скорость реакции окисления в специфических пластовых условиях. [44]
Скорость физико-химической реакции пропорциональна изменению концентрации реагирующих веществ в единицу времени. Если реакция идет в прямом направлении, то концентрация исходных веществ снижается, а продуктов реакции растет, пока не будет достигнуто для данной температур ы термодинамическое равновесие. [45]
Страницы: 1 2 3 4