Изменение - концентрация - электролит
Cтраница 1
Изменение концентрации электролита в прианод-пой зоне зависит от целого ряда факторов, определяемых режимом электролиза, а также от коэффициента диффузии и растворимости электролита. Накопление электролита прямо пропорционально плотности тока и продолжительности электролиза. [1]
Изменение концентрации электролита оказывает незначительное влияние на толщину пленки. С повышением содержания серной кислоты возрастает электропроводность раствора и снижается напряжение в порах пленки, необходимое для получения заданной плотности тока. Вследствие этого уменьшается количество выделяющегося джоулева тепла и, следовательно, уменьшается скорость растворения пленки; с другой стороны повышение концентрации кислоты ускоряет ее растворение. [2]
Зная изменение концентрации электролита в катодном или анодном пространстве, определяют количество электричества, перенесенное теми или другими ионами. [3]
Измеряя изменение концентрации электролита при различных рН, они на разных объектах нашли, что во всех случаях направление движения воды совпадало с направлением движения свободных ионов в жидкости капилляра. [4]
Для изменения концентрации электролитов в растворах путем электродиализа используются ионообменные мембраны - ионообмен - ники в виде пленки. Существуют два типа ионообменных мембран: анионообменные и катионообменные мембраны. Анионообменная мембрана содержит катионные группы, фиксированные в матрице смолы. Заряд фиксированных катионов нейтрализован зарядом подвижных анионов, находящихся в порах смолы. При погружении такой мембраны в раствор электролита анионы раствора могут внедряться в матрицу смолы и замещать первоначально присутствующие в ней анионы, проникновению же катионов препятствуют силы отталкивания их фиксированными в смоле катионами. [5]
Вследствие изменения концентрации электролита при заряде и разряде аккумуляторов его удельный вес также изменяется, поэтому нормальным удельным весом считают тот, который имеет электролит заряженного аккумулятора. [6]
Влияние изменений концентрации электролитов в морской воде ( т.е. разбавленного раствора) на концентрацию рассола показано на фиг. [7]
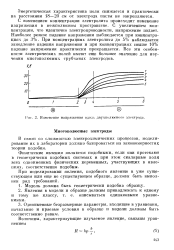 |
Изменение напряжения вдоль двухполюсного электрода. [8] |
С изменением концентрации электролита происходит изменение напряжения в межполюсном пространстве. С увеличением концентрации, что идентично электропроводности, напряжение падает. При концентрациях электролита до 5 % наблюдается замедление падения напряжения и при концентрациях свыше 10 % падение напряжения практически прекращается. Все эти особенности электрических полей имеют еще большее значение для изучения многополюсных трубчатых электродов. [9]
При изменении концентрации электролита порядок его коагулирующего или стабилизирующего действия остается тем же, но интенсивность меняется. [10]
При изменении концентрации электролита порядок его коагулирующего или стабилизирующего действия остается тем же, но интенсивность меняется. [11]
Опыты с изменением концентрации электролита при катодной и анодной поляризации электрода показали, что уменьшение выхода анодного процесса с разбавлением раствора связано с усиленным торможением анодного процесса в этих условиях: пассивация наступает раньше и весь процесс протекает при более положительном и непрерывно меняющемся потенциале. [12]
Электролиз сопровождается изменением концентрации электролита около электродов, что приводит к появлению обратной электродвижущей силы. Это явление называется концентрационной поляризацией. Сущность его состоит в том, что выделение металла на катоде уменьшает около него концентрацию растворенного электролита, а растворение на аноде - увеличивает ее около этого электрода. В результате образуется концентрационный элемент с обратной электродвижущей силой. [13]
Таким образом, изменение концентрации электролита в п раз приводит к изменению ионной силы раствора во столько же раз. Если раствор содержит несколько электролитов в разных концентрациях, то при вычислении ионной силы учитывается вклад всех ионов в ионную силу раствора. [14]
 |
Схема электрофором. [15] |
Страницы: 1 2 3 4